Резюме
Внутрибрюшная гипертензия приводит к бактеремии вследствие нарушения защитных барьеров, полиорганной недостаточности и смерти. Наиболее подробно проблема внутрибрюшной гипертензии исследована в абдоминальной хирургии, у пострадавших с политравмой и у пациентов после операций на аорте. Примерно у половины этих пациентов, находящихся в критическом состоянии, внутрибрюшное давление повышено. Для пациентов с опухолями головного мозга проблема внутрибрюшной гипертензии является фактически неизученной.
Приведенное клиническое наблюдение показывает, что причиной ухудшения состояния у пациента с краниофарингиомой в раннем послеоперационном периоде стал именно вторичный абдоминальный компартмент синдром. Стабилизация состояния отмечалась после нормализации внутрибрюшного давления. В отличие от больных общехирургического профиля, у описанного в статье нейрохирургического пациента комплекс проводимой консервативной терапии, направленной на стимуляцию моторики желудочно-кишечного тракта, сочетался с коррекцией заместительной терапии тиреоидными гормонами.
Таким образом, у нейрореанимационных пациентов возможно развитие внутрибрюшной гипертензии и вторичного абдоминального компартмент синдрома, поэтому у них следует рутинно измерять внутрибрюшное давление. Специфическими для нейрохирургических пациентов причинами повышения внутрибрюшного давления являются тиреоидная недостаточность и повреждение центров регуляции автономной нервной системы. Эти факторы необходимо принимать во внимание при проведении интенсивной терапии нейрореанимационных больных.
Введение
Внутрибрюшная гипертензия (ВБГ) была впервые описана еще в середине XIX века [14]. С тех пор эта проблема неоднократно переживала периоды полного забвения, которые затем сменялись осознанием ее значимости, когда клиницисты и исследователи проводили активный поиск решений для ее своевременной и эффективной коррекции [27,28,34,35,37]. Наиболее подробно проблема ВБГ исследована в абдоминальной хирургии, у пострадавших с политравмой и у пациентов после операций на аорте [7,20,24,29,32,36]. У пациентов с опухолями головного мозга проблема ВБГ является фактически неизученной. Есть единичные работы, в которых было показано, что у пациентов с черепно-мозговой травмой ВБГ может являться непосредственной причиной внутричерепной гипертензии [9,13]. В каких-либо других аспектах проблема ВБГ у нейрохирургических пациентов ранее не рассматривалась.
Мы приводим клиническое наблюдение, в котором у пациента с краниофарингиомой тяжесть состояния в раннем послеоперационном периоде была обусловлена вторичным абдоминальным компартмент синдромом.
Пациент С, 58 лет поступил в Институт Нейрохирургии с диагнозом: Крупная стебельно-интравентрикулярная кистозная краниофарингиома. При поступлении пациент предъявлял жалобы на головную боль, слабость, снижение остроты и сужения полей зрения. Объективно выявлялись грубые мнестические расстройства и дезориентация в месте, времени, личной ситуации. Острота зрения с двух сторон была 0,1. Эндокринные нарушения были представлены ожирением III степени с индексом массы тела 40,5 и гипопитуитаризмом в виде вторичного гипокортицизма, гипотиреоза, гипогонадизма, соматотропной недостаточности. При биохимическом и клиническом исследовании крови патологических изменений выявлено не было. Живот был увеличен в размерах (Рисунок 1).
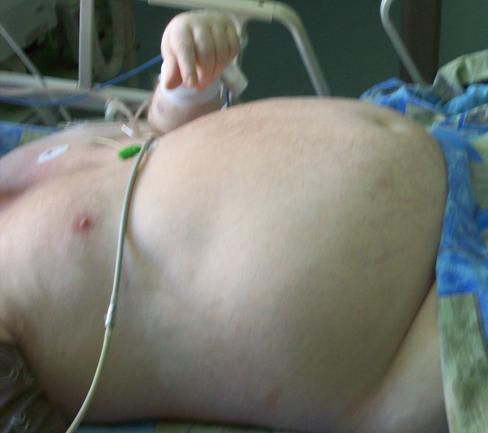
При УЗИ органов брюшной полости и забрюшинного пространства увеличения размеров паренхиматозных органов не было, выявлялись хронические воспалительные изменения печени и поджелудочной железы. Рентгенологически выявлялось усиление легочного рисунка. При МРТ-исследовании головного мозга был подтвержден диагноз крупной кистозной супраселлярной краниофарингиомы (Рисунок 2).
Сопутствующая патология: гепатит С в стадии ремиссии. В качестве первого этапа хирургического лечения было решено установить систему Оммайя в кисту опухоли. Операция произведена под внутривенной анестезией пропофолом и фентанилом. Пробуждение было в обычные сроки, и пациент был экстубирован через 2 часа после завершения операции. В течение четырех суток после операции состояние было стабильным, пациент находился в нейрохирургическом отделении. В послеоперационном периоде уменьшилась выраженность головной боли. Самостоятельное дыхание было адекватным, гемодинамические показатели – стабильными. Пациент ел самостоятельно, кишечные шумы были ослаблены, но нарушений усвоения и пассажа пищи не было. После очистительных клизм был стул. Однократные в течение суток эпизоды полиурии купировались приемом десмопрессина. Системные маркеры воспаления – количество лейкоцитов, лейкоцитарная формула и С-реактивный белок (ЦРП), теипература тела были в пределах нормы (Таблица). Пациенту проводилась инфузионная, гастропротективная, профилактическая антибактериальная и полигормональная заместительная терапия глюкокортикостероидными (гидрокортизон 200 мг/сут), тиреоидными (L-тироксин 200 мкг/сут) и половыми (Омнадрен 250 мг, 1 раз в 2 недели) гормонами. На 5-ые сутки после операции состояние ухудшилось. Развилось сопорозное состояние. При КТ-исследовании головного мозга по сравнению с дооперационным уровнем была выявлена положительная динамика в виде уменьшения размеров желудочковой системы и кисты краниофарингиомы (Рисунок 3).
Базальные цистерны визуализировались хорошо. Гемодинамические показатели оставались в пределах нормы. Появилась одышка. Развился парез желудочно-кишечного тракта: вздутие живота, тошнота, рвота, отсутствие стула и кишечных шумов. Альфа-амилаза и липаза плазмы были в пределах нормы (65 и 34 Ед/л, соответственно). При спиральном КТ-исследовании брюшной полости выявлены раздутые петли кишечника. Поперечный размер живота был практически равен вертикальному, что является признаком выраженной ВБГ (Рисунок 4) [23].
Замедлился темп диуреза до олигоурии. По лабораторным данным, отмечалось существенное нарастание системных маркеров воспаления и повышение уровня мочевины (Таблица). Температура тела оставалась нормальной. Очага инфекции выявлено не было: цитоз ликвора, глюкоза и лактат ликвора, клинический анализ мочи были в пределах нормы, кровь и моча были стерильны при микробиологическом исследовании. Придаточные пазухи носа и основания черепа были воздушны (Рисунок 3).
При спиральном КТ-исследовании грудной клетки синусы были свободны, выявлялись изменения в базальных отделах левого легкого, причину, которых трактовать однозначно было трудно (Рисунок 4).
Эти изменения можно было расценить как пневмонию или ателектаз вследствие элевации диафрагмы и ограничения ее подвижности. Выявлялась диссоциация между незначительными рентгенологическими изменениями, очень высоким уровнем ЦРП, лейкоцитоза, существенным сдвигом лейкоцитарной формулы влево и нормотермией, а также нормальным уровнем прокальцитонина, который всегда повышается при бактериальной пневмонии [8].
Таблица. Динамика клинико-лабораторных параметров в периоперационном периоде.
| До операции | 2 сутки п/о | 5 сутки п/о | 7 сутки п/о | 12 сутки п/о | |
| ВБД (4 измерения в сутки), мм.рт.ст. | ? | ? | 23-20-18-19 | 12-14-14-13 | 9-10-11-10 |
| ДН (одышка, снижение сатурации) | Нет | Нет | Да | Нет | Нет |
| Лейкоцитоз, тыс/мкл | 8,2 | 12,3 | 14,7 | 12,7 | 8 |
| С-реактивный белок, мг/л | 5,3 | 27,6 | 220,6 | 51,8 | 32,4 |
| Сдвиг лейкоцитарной формулы влево | 2% | 3% | 21% | 9% | 7% |
| РСТ (качественный тест) | ? | ? | Отрицательно | Отрицательно | Отрицательно |
| Температура тела (минимальное-максимальное значение в течение суток), °С. | 36,1-36,3 | 36,5-36,8 | 36,0-36,6 | 36,0-36,4 | 35,8-36,6 |
| Мочевина//Креатинин, ммоль/л//мкмоль/л | 4,3/55 | 6,8/65 | 13,8/71 | 6,8/62 | 5,8/74 |
Пациент был переведен в отделение реанимации. При дыхании атмосферным воздухом отмечались эпизоды снижения сатурации до 90-92% и рО2 до 55-60 мм.рт.ст, но на фоне инсуффляции кислорода нарушений газового состава артериальной крови не было. При измерении внутрибрюшного давления (ВБД) через мочевой катетер оно составило 23 мм.рт.ст, что соответствовало выраженной ВБГ. В дальнейшем, в течение всего времени пребывания пациента в отделении реанимации производилось дискретное, каждые 6 часов, измерение ВБД также через мочевой катетер при помощи методики, описанной Manu Malbrain [23]. Причиной ВБГ, по-видимому, был парез желудочно-кишечного тракта на фоне морбидного ожирения. Была начата терапия, направленная на стимуляцию перистальтики желудочно-кишечного тракта: вазелиновое масло, солевые растворы со скоростью 40-60 мл/час в зонд, антихолинэстеразные препараты, метоклопрамид и эритромицин внутривенно, двукратные в сутки очистительные клизмы. Было начато парентеральное питание трех-компонентной смесью Нутрифлекс (BBraun, Германия), и корригирована гастропротективная терапия – Н2-блокаторы заменены блокаторами протонной помпы. Вместе с этим была корригирована терапия тиреоидными гормональными препаратами. К терапии L-тироксином в дозе 200 мкг/сут был добавлен тиреокомб в дозе 2 таблетки в сутки, поскольку при исследовании уровня гормонов в плазме определялся низкий уровень Т3 и свТ3. Не смотря на отсутствие очевидного очага инфекции эмпирически был назначен Сульперазон. В течение суток удалось добиться усвоения глюкозо-солевых растворов и незначительного снижения ВБД. Однако ВБГ сохранялась, поэтому было принято решение о проведении продленной эпидуральной анестезии. Эпидуральный катетер был установлен на уровне Th9-Th10 и проведен в краниальной направлении на 5 см. Начато постоянное введение ропивакаина в дозе 20 мг/час, продолжавшееся в течение 7 суток. ВБД начало снижаться в течение первых 12 часов, а нормализовалось через 1,5 суток после начала эпидуральной инфузии. На фоне коррекции структуры терапии тиреоидными препаратами, продолжавшейся терапии, направленной на стимуляцию желудочно-кишечного тракта и эпидуральной анестезии удалось добиться нормализации стула. Кроме этого, удалось купировать одышку. Через двое суток системные маркеры воспаления начали снижаться, темп диуреза восстановился, а уровень мочевины нормализовался. Гемодинамические параметры были стабильными. Температура тела оставалась нормальной. Парентеральное питание было прекращено, и было начато энтеральное. К 12 суткам после операции (7 сутки пребывания пациента в отделении реанимации) состояние пациента стабилизировалось, системные маркеры воспаления вместе с показателями ВБД нормализовались. При повторном спиральном КТ-исследовании грудной клетки была выявлена положительная динамика, вероятно, связанная с улучшением механики дыхания, увеличением подвижности диафрагмы и разрешением ателектазирования на фоне регресса гипостатических явлений в задне-нижних отделах легких (Рисунок 5).
Быстрый, в течение недели, регресс рентгенологических изменений в легких – это еще один фактор, который свидетельствует в пользу ателектазирования на фоне ВБГ, а не в пользу пневмонии. Повышение же маркеров системного воспаления при ухудшении состояния, наиболее вероятно, было обусловлено бактеремией. Эпидуральный катетер был удален на 7 сутки после его установки. Пациент был переведен в нейрохирургическое отделение на следующий день. Реабилитационные мероприятия позволили добиться дальнейшего улучшения состояния. С учетом состояния пациента, МРТ-картины, возраста и характера сопутствующей патологии от удаления опухоли было решено отказаться. Пациент был выписан из Института на 21 сутки после операции в удовлетворительном состоянии.
Обсуждение
ВБД в норме не превышает 10 мм.рт.ст. Внутрибрюшной гипертензией (ВБГ) считается повышение ВБД выше 12 мм.рт.ст. Выделяют 4 степени ВБГ: I степень: 12-15 мм.рт.ст, II степень: 16-20 мм.рт.ст, III степень: 21-25 мм.рт.ст, IV степень: >25 мм.рт.ст. [26]. Как минимум у половины пациентов, находящихся в критическом состоянии, ВБД повышено [17]. ВБГ приводит к бактеремии, полиорганной недостаточности (ПОН) и смерти [4,17]. ВБГ III-IV степени, вместе с наличием ПОН, являются критериями абдоминального компартмент синдрома (АКС), который разделяется на первичный, вторичный и третичный [26]. Первичный АКС развивается у пациентов с патологией органов брюшной полости и забрюшинного пространства, вторичный – у пациентов без абдоминальной патологии, третичный – у пациентов, перенесших декомпрессивную лапаротомию, выполненную в связи с первичным или вторичным АКС [26]. При первичном и третичном АКС показаны раннее хирургическое устранение причины, вызвавшей ВБГ и ранняя декомпрессивная лапаротомия. Причинами вторичного АКС являются сепсис, синдром капиллярной утечки, обширная ожоговая травма, массивная инфузионно-трансфузионная терапия [3,17,18]. При этом показана, прежде всего, консервативная терапия, заключающаяся в коррекции факторов, приведших к повышению ВБД, стимуляции моторики желудочно-кишечного тракта (ЖКТ) и проведении эпидуральной аналгезии на нижнегрудном уровне [15,22,30]. Стимуляция моторики ЖКТ проводится с помощью энтерального введения солевых растворов, по возможности, раннего начала энтерального кормления, внутривенного использования метоклопрамида и эритромицина [11,16,22]. Была показана эффективность кормления через назоеюнальный зонд [1]. Отдельной терапевтической опцией, которой следует поддерживаться при лечении любого АКС, яыляется поддержание абдоминального перфузионного давления (АПД) выше 50 мм.рт.ст. АПД является разницей между ВБД и средним артериальным давлением. В ряде исследований было показано, что снижение АПД ниже 50 мм.рт.ст. приводит к ухудшению результатов лечения пациентов с АКС [12]
Наиболее полно изучен первичный и третичный АКС [12,19]. Данных о вторичном АКС, особенно в нейрохирургической практике, фактически нет. Существуют отдельные работы, в которых изучалась роль ВБГ у нейрохирургических пациентов. Было показано, что при ВБГ возрастает внутричерепное давление вследствие повышения внутригрудного давления и ухудшения на этом фоне венозного оттока из полости черепа [9,13]. Кроме этого, описан феномен ухудшения резорбции ликвора при ВБГ, что также приводит к повышению ВЧД [33]. Безусловно, при лечении нейрореанимационного пациента с внутричерепной гипертензией существует вероятность ее агравации на фоне внутрибрюшной гипертензией. Однако комплекс интенсивной терапии ВЧГ, включающий применение седативных препаратов, миорелаксантов, поддержание адекватного среднего артериального давления, проведение раннего энтерального питания, одновременно соответствует и рекомендациям по борьбе с ВБГ [10,12,15,22,30].
У нейрореанимационного пациента, в отличие от больных без повреждения центральной нервной системы, существуют дополнительные причины для развития ВБГ. Функция ЖКТ регулируется диэнцефальными структурами и эндокринной системой [6,38]. Гормоны щитовидной железы оказывают непосредственное влияние на функцию ЖКТ [38]. Гипотиреоз, как правило, в рамках гипопитуитаризма развивается в 8,5-55% наблюдений у разных групп нейрохирургических пациентов и приводит к развитию пареза ЖКТ [2,21,31]. Повреждение диэнцефальных структур также приводит к парезу ЖКТ. Парез ЖКТ вызывает ВБГ. Поэтому среди всей нейрохирургической патологии при опухолях хиазмально-селлярной области риск развития ВБГ вследствие пареза ЖКТ наиболее высокий, поскольку диэнцефальные структуры изначально вовлечены в патологический процесс и у подавляющего большинства этих больных есть тиреоидная недостаточность. С одной стороны, развитие ВБГ у этих пациентов отражает тяжесть повреждения гипоталамо-гипофизарной системы, а с другой стороны, сформировавшийся абдоминальный компартмент синдром приводит к органной недостаточности и повышает ВЧД. Это еще больше ухудшает состояние пациента. Формируется порочный круг, который невозможно прервать без нормализации ВБД. Вместе с этим при некомпенсированной тиреоидной недостаточности и/или при повреждении диэнцефальных структур невозможно нормализовать ВБД.
В приведенном наблюдении ухудшение состояния началось с развития пареза ЖКТ, очень быстро приведшего к развитию выраженной ВБГ. Далее развилась дыхательная недостаточность, олигоурия, существенно возрос уровень маркеров воспаления – ЦРП, лейкоцитоза, сдвига лейкоцитарной формулы влево. Это свидетельствовало о формировании вторичного АКС. Проведение комплекса мероприятий, направленных на борьбу с парезом ЖКТ и ВБГ, в том числе эпидуральная анестезия, позволили снизить ВБД. Принципиально важным аспектом в лечении этого пациента, в отличие от больных, не имеющих тиреоидной недостаточности, явилась коррекции схемы проводимой гормональной терапии. Поскольку не смотря на прием L-тироксина в дозе 200 мкг/сут, у пациента сохранялись низкие уровни Т3 и свТ3, к терапии был добавлен тиреокомб – препарат, содержащий и тироксин (Т4), и трийодтиронин (Т3). Кроме этого, на протяжении всего времени пребывания пациента в отделении реанимации уровень среднего артериального давления тщательно контролировался для поддержания АПД выше 50 мм.рт.ст. После купирования ВБГ у пациента нормализовались уровни системных маркеров воспаления, восстановился адекватный темп диуреза, были купированы признаки дыхательной недостаточности.
Заключение
У нейрохирургических больных даже без какой-либо сопутствующей абдоминальной патологии возможно развитие внутрибрюшной гипертензии и вторичного абдоминального компартмент синдрома, поэтому у таких больных следует рутинно измерять внутрибрюшное давление. Специфическими для нейрохирургических пациентов причинами повышения внутрибрюшного давления являются тиреоидная недостаточность и повреждение диэнцефальных структур. Эти факторы необходимо принимать во внимание при проведении интенсивной терапии нейрореанимационных пациентов.
Литература
- Acosta-Escribano J, Ferna´ndez-Vivas M, Grau Carmona T, et al. Gastric versus transpyloric feeding in severe traumatic brain injury: a prospective, randomized trial. // Intensive Care Med, 2010; on-line first: DOI 10.1007/s00134-010-1908-3.
- Aimaretti G, Ambrosio MR, Di Somma C, et al. Traumatic brain injury and subarachnoid haemorrhage are conditions at high risk for hypopituitarism: screening study at 3 months after the brain injury. // Clin Endocrinol 2004; 61:320-6.
- Balogh Z, McKinley BA, Cocanour CS, et al. Supranormal trauma resuscitation causes more cases of abdominal compartment syndrome. // Arch Surg. 2003;138:637-42; discussion 642-3.
- Balogh Z, McKinley BA, Holcomb JB et al. Both primary and secondary abdominal compartment syndrome can be predicted early and are harbingers of multiple organ failure. // J Trauma 2003; 54:848-859, discussion 859-861.
- Balogh Z, Moore FA. Postinjury secondary abdominal compartment syndrome. From Abdominal compartment syndrome, edited by Ivatury RR, Cheatham ML, Malbrain M, Sugrue. 2006, Landes Bioscience, Texas.
- Bauer AJ, Boeckxstaens GE Mechanisms of postoperative ileus. // Neurogastroenterol Motil. 2004; 16 Suppl 2:54-60.
- Biancofiore G, Bindi ML, Romanelli AM, et al. Intra-abdominal pressure monitoringin liver transplant recipients: A prospective study. // Intensive Care Med 2003; 29:30-36.
- Blasi F, Stolz D, Piffer F. Biomarkers in lower respiratory tract infections. // Pulm Pharmacol Ther. 2010; 29:Epub ahead of print.
- Bloomfield GL, Ridings PC, Blocher CR et al. A proposed relationship between increased intra-abdominal, intrathoracic, and intracranial pressure. // Crit Care Med 1997; 25:496-503.
- Brain Trauma Foundation, American Association of Neurological Surgeons, Congress of Neurological Surgeons. Guidelines for the management of severe traumatic brain injury. // Cerebral perfusion thresholds. J Neurotrauma 2007;24:S59-S64.
- Carlson GL, Dark P. Acute intestinal failure. // Curr Opin Crit Care. 2010; 19:Epub ahead of print.
- Cheatham ML, Malbrain M. Abdominal perfusion pressure. From Abdominal compartment syndrome, edited by Ivatury RR, Cheatham ML, Malbrain M, Sugrue. 2006, Landes Bioscience, Texas.
- Citerio G, Vascotto E, Villa F et al. Induced abdominal compartment syndrome increases intracranial pressure in naerotrauma patients: A prospective study. // Crit Care Med 2001; 29:1466-1471.
- Emerson H. Intra-abdominal pressures. // Arch Intern Med. 1911; 7:754-784.
- Freise H, Fischer LG. Intestinal effects of thoracic epidural anesthesia. // Curr Opin Anaesthesiol. 2009; 22(5):644-8.
- Fruhwald S, Holzer P, Metzler H Intestinal motility disturbances in intensive care patients pathogenesis and clinical impact. // Intensive Care Med 2007; 33:36–44.
- Gallagher JJ. Intra-abdominal hypertension: detecting and managing a lethal complication of critical illness. // AACN Adv Crit Care. 2010; 21:205-19.
- Ivy ME, Atweh NA, Palmer J, et al. Intra-abdominal hypertension and abdominal compartment syndrome in burn patients. // J Trauma. 2000; 49:387-91.
- Ivy ME. Secondary abdominal compartment syndrome in burns. From Abdominal compartment syndrome, edited by Ivatury RR, Cheatham ML, Malbrain M, Sugrue. 2006, Landes Bioscience, Texas.
- Kopelman T, Harris C, Miller R et al. Abdominal compartment syndrome in patients with isolated extraperitoneal injuries. // J Trauma 2000; 49:744-749.
- Kreitschmann-Andermahr I. Subarachnoid hemorrhage as a cause of hypopituitarism. // Pituitary 2005; 8:219-225.
- Lal S, Teubner A, Shaffer JL. Review article: intestinal failure. // Aliment Pharmacol Ther. 2006; 24:19-31.
- Malbrain M, Jones F. Intra-abdominal pressure measurement techniques. From Abdominal compartment syndrome, edited by Ivatury RR, Cheatham ML, Malbrain M, Sugrue. 2006, Landes Bioscience, Texas.
- Maxwell RA, Fabian TC, Croce MA et al. Secondary abdominal compartment syndrome: an underappreciated manifestation of sever hemorrhagic shock. // J trauma 1999; 47:995-999.
- Mayberry JC. Prevention of abdominal compartment syndrome. From Abdominal compartment syndrome, edited by Ivatury RR, Cheatham ML, Malbrain M, Sugrue. 2006, Landes Bioscience, Texas.
- Muckart DJJ, Ivanury RR, Leppaniemi A, Smith RS. Definitions. From Abdominal compartment syndrome, edited by Ivatury RR, Cheatham ML, Malbrain M, Sugrue. 2006, Landes Bioscience, Texas.
- Olerud S. Experimental studies on portal circulation at increased intre-abdominal pressure. // ACTA Physio Scan. 1953; 30(Supp 109):4-93.
- Overholt RH. Intraperitoneal pressure. // Arch Surg. 1931; 22:691-703.
- Papavassiliou V, Anderton M, Loftus IM et al. The physiological effects of intra-abdominal pressure following aneurysm repair. // Eur J Vasc Endovasc Surg 2003; 26:293-298.
- Parr MJA, Olvera CI. Medical management of abdominal compartment syndrome. From Abdominal compartment syndrome, edited by Ivatury RR, Cheatham ML, Malbrain M, Sugrue. 2006, Landes Bioscience, Texas.
- Popugaev KA, Savin IA, Goriachev AS, Kadashev BA. Hypothalamic injury as a cause of refractory hypotension after sellar region tumor surgery. // Neurocrit Care 2008; 8:366–373.
- Rasmussen TE, Hallett JW, Noel AA et al. Early abdominal closure with mesh reduces multiple organ failure after ruptured abdominal aortic aneurysms repair: guidelines from a 10 year case-control study. // J Vasc Surg 2002; 35:246-253.
- Rosenthal RJ, Hiatt JR, Phillips EH, et al. Intracranial pressure. Effects of pneumoperitoneum in a large-animal model. // Surg Endosc. 1997; 11:376-380.
- Richardson JD, Trinkle JK. Hemodynamic and respiratory alterations with increased intra-abdominal pressure. // J Surg Res. 1976; 20:401-404.
- Schein M, Wittmann DH, Aprahamian CC, et al. The abdominal compartment syndrome: The physiological and clinical consequences of elevated intra-abdominal pressure. // J Am Coll Surg. 1995; 180:745-753.
- Sugrue M, Jones F, Deane SA et al. Intra-abdominal hypertension is an independent cause of postoperative renal impairment. // Arch Surg 1999; 134:1082-1085
- Thorington JM, Schmidt CF. A study of urinary output and blood-pressure changes resulting in experimental ascites. // Am J Med Sci. 1923; 165:880-890
- Wiersinga WM. Hypothyroidism and myxedema coma. From Endocrinology, edited by DeGroot LJ, Jameson JL, 5th edition, 2006, Elsevier Saunders. ISBN 0-7216-0376-9






