Симптоматическая эпилепсия наблюдается у 20—80% больных с опухолями головного мозга [1, 2]. В подавляющем большинстве случаев эпилептические приступы возникают до операции и к моменту ее проведения больные уже получают противосудорожную терапию, которая продолжается и после нейрохирургического вмешательства. При отсутствии приступов в анамнезе профилактическая противосудорожная терапия в настоящее время не назначается [3]. В этой связи особую проблему представляют эпилептические приступы, которые впервые развиваются после нейрохирургической операции (приступы de novo). С одной стороны, эти приступы могут быть спровоцированы самим фактом операции и самостоятельно прекратиться без противосудорожной терапии, с другой — могут быть дебютом симптоматической эпилепсии, что требует длительной медикаментозной терапии. Единого алгоритма принятия решения в таких ситуациях не существует. Одни авторы предлагают в любом случае начинать противосудорожную терапию [4, 5], другие, в соответствии со стандартами эпилептологии, рекомендуют начинать лечение лишь после постановки диагноза «симптоматическая эпилепсия» [3].
Очевидно, что необоснованное назначение противосудорожной терапии значительно снижает качество жизни пациента. Если же впервые развившийся после операции эпилептический приступ является проявлением симптоматической эпилепсии, то отсутствие терапии приведет к развитию осложнений и ухудшит прогноз [2, 3]. Помощь в принятии решения может оказать видеоэлектроэнцефалографический мониторинг (видео-ЭЭГ-мониторинг).
Мы представляем два клинических наблюдения, в которых видео-ЭЭГ-мониторинг повлиял на выбор тактики дальнейшего ведения больных.
Наблюдение 1. У пациентки 70 лет за 2 мес до госпитализации появилась и стала нарастать слабость в левых конечностях, ухудшилась память на текущие события, снизилась критика собственного состояния. При магнитно-резонансной томографии (МРТ) была диагностирована внутримозговая опухоль правой височной доли с зоной перифокального отека (рис. 1).
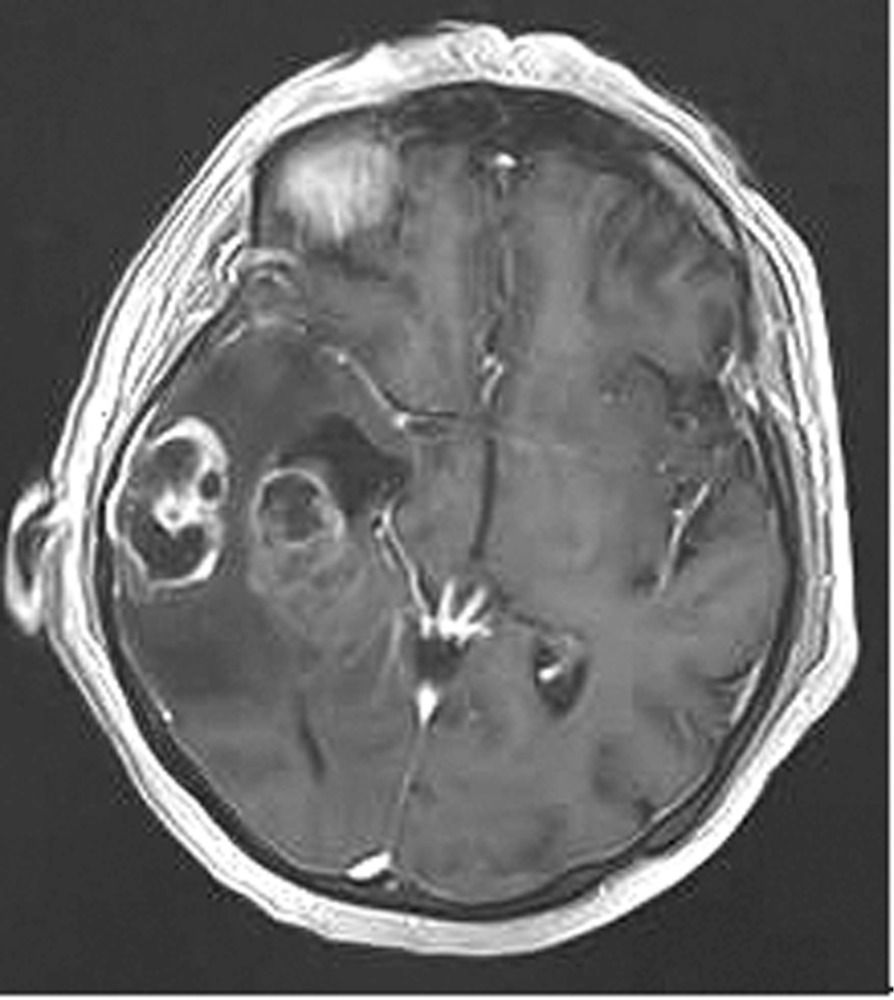
Рис. 1. Наблюдение 1. МРТ перед операцией. Внутримозговая опухоль правой височной доли с зоной перифокального отека. Опухоль, оказавшаяся при гистологическом исследовании глиобластомой (Grade IV), удалена 02.02.16. После операции пациентка была переведена в палату пробуждения отделения реанимации, где спустя 4,5 ч (через 2 ч после экстубации) развился вторичный генерализованный судорожный приступ продолжительностью около 2 мин. Приступ был купирован внутривенным болюсным введением диазепама 10 мг и вальпроевой кислоты (конвулекс) 500 мг. Экстренное КТ-исследование выявило послеоперационные изменения правой височной доли и отсутствие хирургических осложнений (рис. 2).
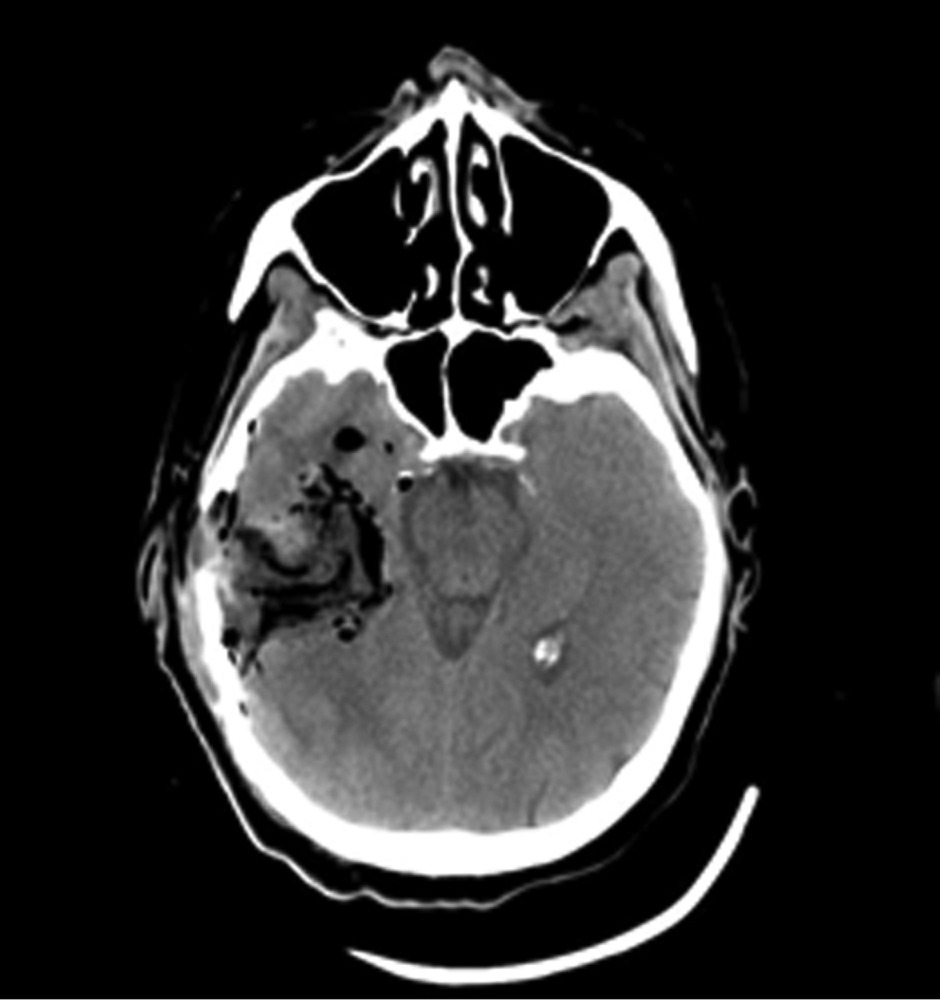
Рис. 2. Наблюдение 1. СКТ в 1-е сутки после удаления опухоли правой височной доли. Выявлены послеоперационные изменения в зоне хирургического вмешательства. Пациентке в 1-е сутки после операции проводился видео-ЭЭГ-мониторинг, где на фоне дезорганизации коркового ритма было выявлено замедление биопотенциалов в правой лобно-височной области (рис. 3). За следующие 13 ч записи было зарегистрировано 7 электроэнцефалографических паттернов длительностью от 2 до 4 мин, сопровождающихся появлением эпилептиформных потенциалов в виде комплексов острая—медленная волна в правой лобно-центрально-височной области (рис. 4). Шесть из семи эпизодов не проявлялись клинически. В 1 случае пароксизмальная симптоматика проявилась кратковременным (около 5 с) тоническим напряжением мышц шеи и поворотом головы вправо.
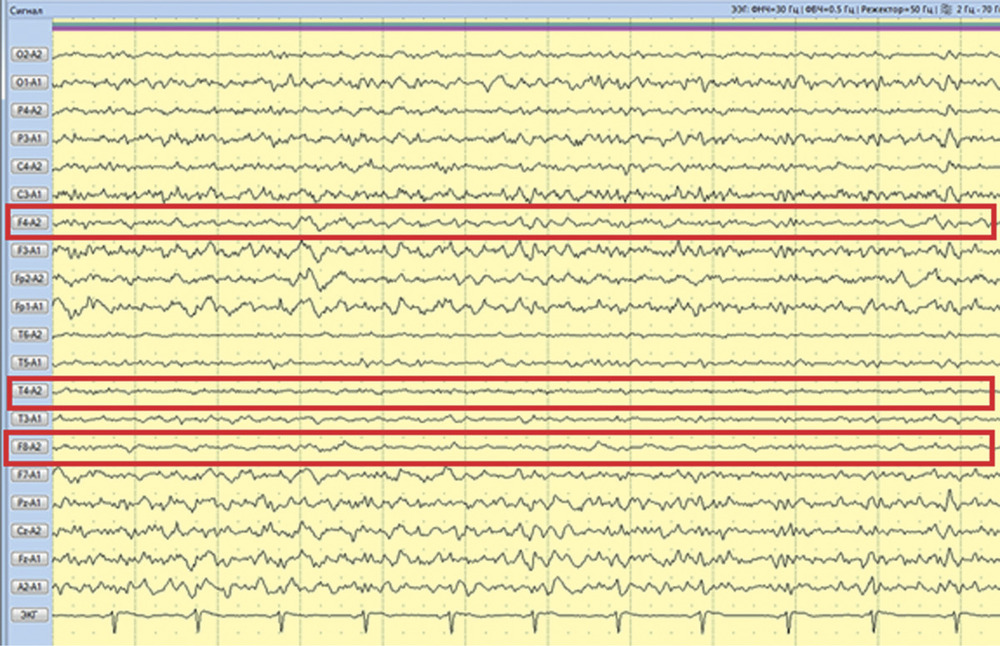
Рис. 3. Наблюдение 1. Фрагмент 13-часового ЭЭГ-мониторинга. Диффузное снижение амплитуды биопотенциалов мозга. Замедление в правой лобно-височной области на дезорганизованном фоне. Типичная эпилептиформная активность не регистрируется.
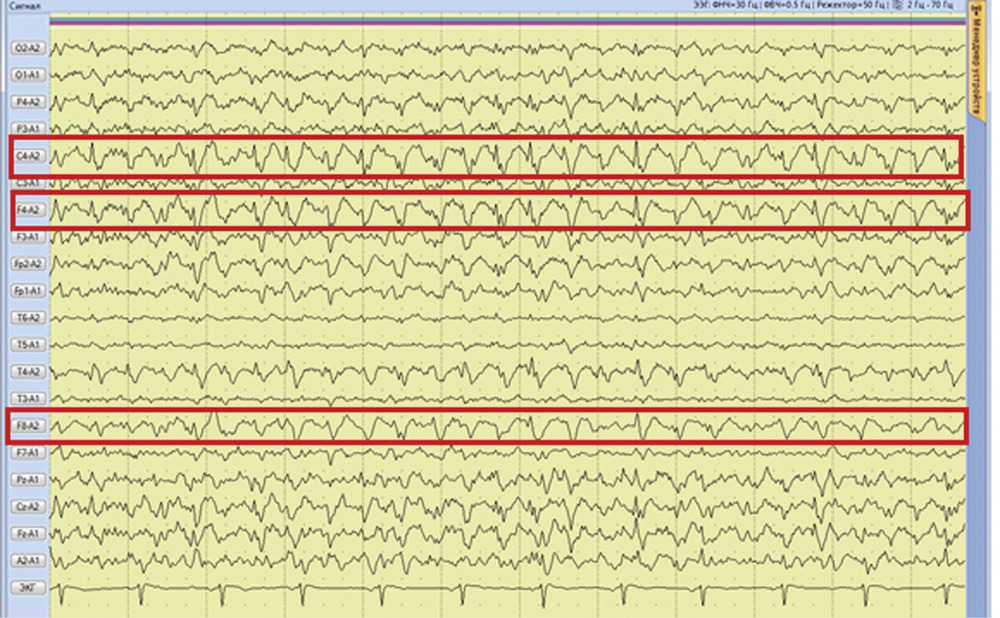
Рис. 4. Наблюдение 1. Фрагмент 13-часового ЭЭГ-мониторинга. Эпилептиформные потенциалы в виде комплексов острая—медленная волна в правой лобно-центрально-височной области. Учитывая данные видео-ЭЭГ-мониторинга, пациентке была назначена противосудорожная терапия в виде внутривенного введения вальпроевой кислоты (конвулекс) через перфузор в дозе 1500 мг/сут. На 2-е сутки после операции эпилептиформная активность на ЭЭГ прекратилась, больная переведена в клиническое отделение, где была продолжена противосудорожная терапия вальпроевой кислотой (конвулекс) в таблетированной форме в дозе 2000 мг/сут. Через 11 дней после операции пациентка в удовлетворительном состоянии выписана из клиники с рекомендацией продолжить прием 1500 мг/сут вальпроевой кислоты под контролем ЭЭГ и концентрации препарата в плазме крови.
Наблюдение 2. Пациентка 64 лет за 10 мес до настоящей госпитализации была оперирована и проходила комбинированное лечение по поводу глиобластомы (Grade IV) левой лобной доли. В течение всего срока заболевания приступов с нарушением сознания или иных пароксизмальных состояний не наблюдалось. Противосудорожную терапию не получала. При контрольной МРТ за 3 нед до госпитализации выявлено увеличение размеров опухоли. Принято решение о повторном хирургическом вмешательстве. После операции 14.03.16 пациентка была переведена в палату пробуждения, где спустя 1,5 ч на фоне выхода из наркозного сна развился вторичный генерализованный судорожный приступ, который самостоятельно купировался в течение 1 мин. Проведенное КТ-исследование выявило послеоперационные изменения и отсутствие хирургических осложнений (рис. 5). В ходе суточного видео-ЭЭГ-мониторинга были выявлены диффузные изменения биопотенциалов в виде умеренновыраженной дезорганизации корковой активности, при отсутствии типичных эпилептиформных потенциалов (рис. 6). Было принято решение не назначать больной противосудорожную терапию и оставить ее на сутки под наблюдением в отделении реанимации. Клинических приступов или иных пароксизмальных проявлений не отмечено, при видео-ЭЭГ-мониторинге эпилептиформная активность не зафиксирована. После перевода в клиническое отделение приступов также не наблюдалось. Спустя 8 дней после операции пациентка в удовлетворительном состоянии выписана для продолжения химиотерапии по месту жительства.
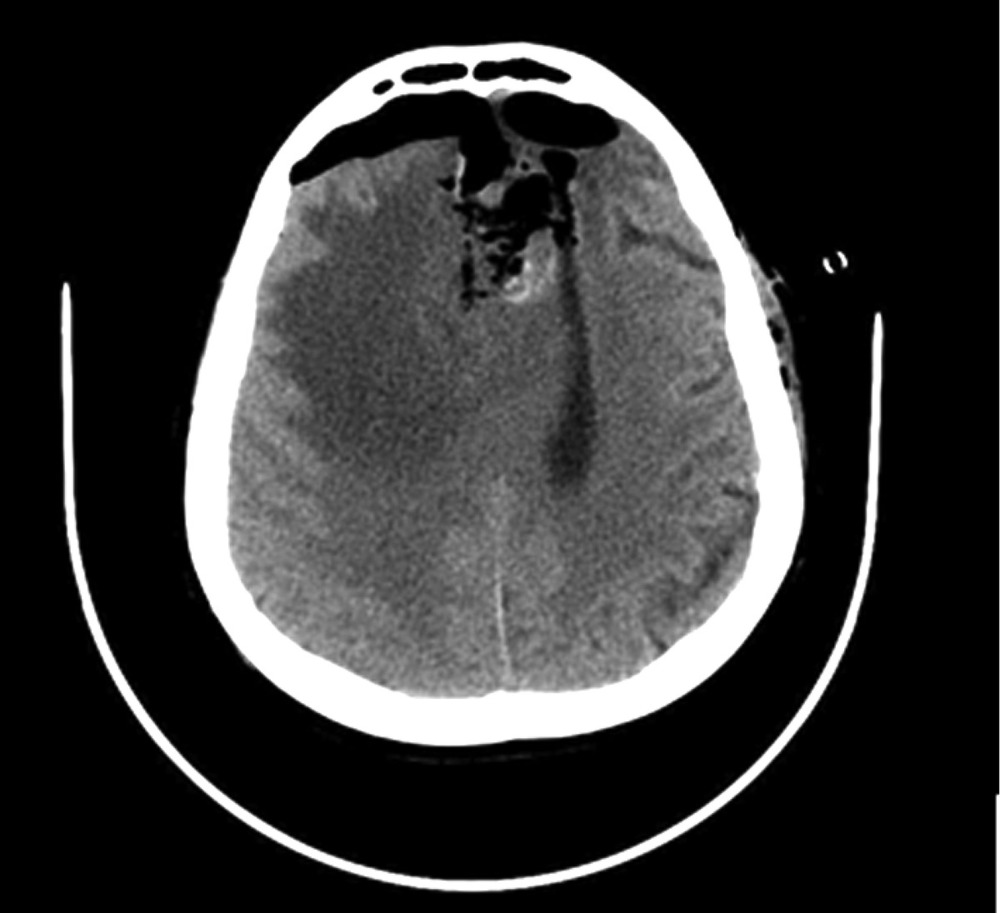
Рис. 5. Наблюдение 2. СКТ в 1-е часы после удаления опухоли левой лобной доли. Послеоперационные изменения с зоной перифокального отека, скопления воздуха и небольшой зоной имбибиции кровью в области операции.
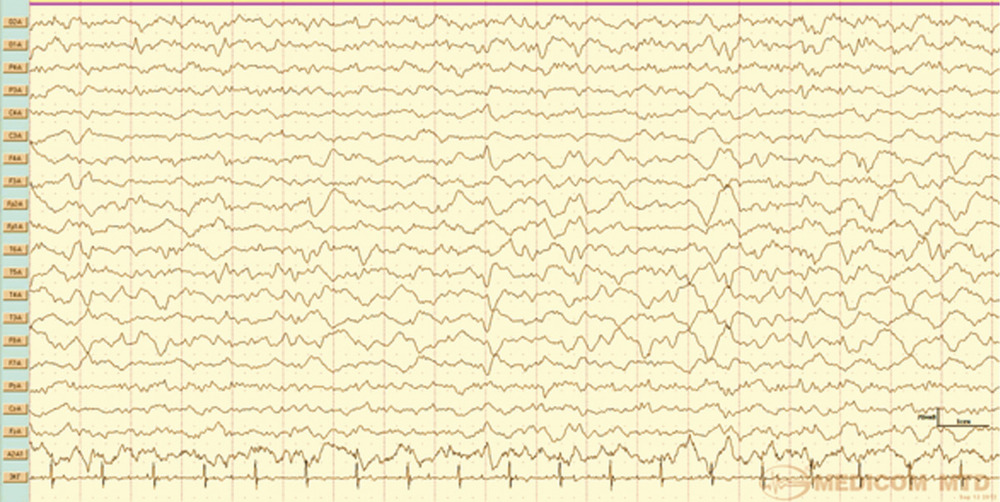
Рис. 6. Наблюдение 2. Фрагмент ЭЭГ-мониторинга. Умеренновыраженный дезорганизованный фон, с преобладанием медленных форм активности и острых потенциалов в лобно-передневисочной области, больше справа. Обсуждение Впервые возникшие эпилептические приступы (de novo) в зависимости от срока их развития после операции разделяют на ранние (acute postoperative seizures) и поздние [6, 7]. К ранним приступам как правило, относят те, которые возникают в течение 48 ч после операции, но ряд авторов считают, что к ранним эпилептическим приступам следует относить все приступы, возникающие в 1-ю неделю после операции [8].
Частота ранних впервые возникших приступов после удаления опухоли мозга варьирует в разных сериях наблюдений от 4,3 до 23,6% [7, 9] и зависит от локализации, гистологического диагноза, удаленного объема, выраженности отека, геморрагической имбибиции мозга, пневмоцефалии и наличия осложнений [6, 9]. В среднем считается, что вероятность возникновения эпилептических приступов после удаления полушарной опухоли составляет 5—10% [7, 9].
Патогенез впервые возникших в раннем после-операционном периоде эпилептических приступов окончательно не установлен. Одним из механизмов может быть раздражение коры мозга компонентами крови и продуктами распада гемоглобина. Возможно также, что накапливающиеся в очаге повреждения перекисные соединения снижают концентрацию гамма-аминомасляной кислоты, которая ингибирует нейрональную активность коры и таламуса [6]. Наконец, в ишемизированной перитуморозной ткани мозга за счет снижения синтетаз АТФ нарушается трансмембранный транспорт воды и ионов, что приводит к изменению потенциала клеточной мембраны [11]. В любом случае патогенез впервые возникших ранних послеоперационных приступов обусловлен механизмами, действие которых, как правило, прекращается в раннем послеоперационном периоде. Соответственно такие приступы, особенно единичные, не дают оснований диагностировать симптоматическую эпилепсию и должны расцениваться как реакция мозга на хирургическое вмешательство [6, 8].
В ряде исследований [6, 11] показано, что ранние впервые возникшие послеоперационные приступы не повышают риск развития симптоматической эпилепсии и не являются поводом для назначения противосудорожной терапии. Менее распространено мнение о том, что приступы в раннем послеоперационном периоде увеличивают риск развития послеоперационной симптоматической эпилепсии [12].
Профилактическое2 назначение противосудорожных средств после нейрохирургических вмешательств широко практиковалось в ХХ веке и сегодня рутинно осуществляется во многих отечественных и зарубежных клиниках. Вопрос о профилактическом применении противосудорожных препаратов в настоящее время остается дискуссионным. Обзор Американской ассоциации нейрохирургов (AANS) за 2005 г. показал, что чаще противосудорожные препараты для профилактики используют длительно практикующие нейрохирурги [13]. Некоторые авторы [14] предлагают для профилактики ранних приступов назначение противосудорожных препаратов в первую неделю после операции. Комитет качества и стандартизации Американской академии неврологов (AAN) в рекомендациях 2000 г. не рекомендует продолжать противосудорожную терапию дольше одной недели после операции, так как медикаментозная профилактика неэффективна для предотвращения развития позднего приступа [15].
Всего, по данным литературы [17], проведено 5 рандомизированных контролируемых испытаний трех противоэпилептических препаратов: фенитоина, фенобарбитала и вальпроатов. Разницы между действием этих средств и плацебо относительно предотвращения первого приступа у пациентов с опухолями головного мозга не выявлено. Более того, в одном исследовании результаты в группе больных, профилактически получавших фенитоин, оказались хуже, чем в группе плацебо (10 и 8% ранних послеоперационных приступов соответственно), причем побочные эффекты препарата отмечены у 18% получавших его пациентов [17]. Следует подчеркнуть, что исследования высшего уровня доказательности проведены только по трем упомянутым препаратам, и нет оснований предполагать аналогичный результат при изучении новых противосудорожных средств.
В литературе [17, 18] доминирует мнение, что побочные эффекты профилактической противосудорожной терапии превосходят возможную пользу и однозначно снижают качество жизни больных. Очевидно, что в определенных ситуациях ранние послеоперационные приступы бывают первым проявлением симптоматической эпилепсии и промедление с назначением соответствующей терапии может иметь негативные последствия. Дифференциальный диагноз между ранними послеоперационными приступами, возникшими как реакция мозга на повреждение, и ранними приступами, являющимися дебютом симптоматической эпилепсии, затруднен, и однозначного алгоритма принятия решения в такой ситуации в современной литературе не представлено.
Методом, помогающим принять верное решение, служит видео-ЭЭГ-мониторинг. Продолженный видео-ЭЭГ-мониторинг более информативен по сравнению с рутинной записью ЭЭГ [3, 19]. Мы использовали рекомендации ESICM (Европейское общество интенсивной терапии) по проведению видео-ЭЭГ-мониторинга в отделениях нейрореанимации [19]. В соответствии с ними видео-ЭЭГ-мониторинг проводили сразу после выявления приступа.
В настоящее время в нашей клинике используется стандарт терапии продолженного эпилептического приступа и эпилептического статуса [18], согласно которому препаратом первой линии (из зарегистрированных в России) являются бензодиазепины (диазепам 0,1—0,3 мг/кг). Препаратами второй линии могут быть вальпроевая кислота или леветирацетам. Вальпроевая кислота (конвулекс) вводится внутривенно болюсно в дозе 15 мг на 1 кг массы тела, а далее через 30 мин, через перфузор в дозе 1 мг/кг/ч (не более 2500 мг/сут). Леветирацетам (кеппра) вводится в дозе 30 мг/кг/сут внутривенно болюсно, дозу разделяют на три приема (не более 3000 мг/сут). При однократно возникшем эпилептическом приступе, даже самостоятельно прекратившемся, проводится видео-ЭЭГ-мониторинг. Части больных, с учетом результатов мониторинга в дальнейшем назначается противосудорожная терапия на срок не менее 1 года, под контролем ЭЭГ и МРТ. Другая часть пациентов без явной эпилептической активности, по данным ЭЭГ-мониторинга, выписывается под наблюдение невролога без назначения противосудорожной терапии, с последующим динамическим МРТ- и ЭЭГ-контролем. При повторно возникающих приступах назначается противосудорожная терапия.
Заключение
На основании анализа данных литературы можно говорить о том, что развитие эпилептических приступов de novo после нейрохирургических вмешательств — нередкое явление, требующее не только быстрой реакции врача для купирования приступа, но и осмысления ситуации относительно дальнейшего ведения пациента. Развитие симптоматической эпилепсии может привести к ухудшению исходов хирургического лечения, повышению летальности, увеличению срока пребывания пациента в стационаре. С другой стороны, неоправданное использование противоэпилептических препаратов в ситуации, когда единственный приступ является реакцией мозга на операционную травму, существенно снижает в дальнейшем качество жизни пациента. Дискуссия, имеющая место на сегодняшний день в литературе, подтверждает нерешенность этих проблем (это касается и профилактического назначения препаратов, и выбора конкретного противоэпилептического средства, и сроков его использования).
Приведенные нами клинические наблюдения отражают различные варианты подхода к терапии впервые развившихся эпилептических приступов у пациентов после удаления внутримозговой опухоли. По нашему мнению, одним из важных на сегодняшний день критериев для принятия решения о назначении противосудорожной терапии являются данные видео-ЭЭГ-мониторинга, который необходимо проводить после однократно возникшего эпилептического приступа в первую неделю после операции.
Авторы заявляют об отсутствии конфликта интересов.
Комментарий
Статья посвящена актуальной проблеме — тактике ведения пациентов с эпилептическими приступами denovo после удаления внутримозговых опухолей. Ведение пациентов с так называемыми «острыми симптоматическими приступами» является предметом активных обсуждений в последние годы. Казалось бы все просто: возникли эпилептические приступы у больных с поражением головного мозга — необходимо длительное назначение антиэпилептических препаратов. Однако это далеко не так и не во всех случаях.
Авторы приводят два клинических наблюдения. У обеих пациенток после удаления злокачественных опухолей головного мозга развились билатеральные тонико-клонические эпилептические приступы. В первом случае при проведении видео-ЭЭГ мониторинга (ВЭМ) было выявлено региональное замедление, эпилептиформная активность и множественные ЭЭГ паттерны фокальных приступов. Во втором — лишь однократный приступ с отсутствием эпилептиформной активности на ЭЭГ. В первом случае авторы рекомендовали длительный прием антиэпилептических препаратов, во втором — только наблюдение.
Таким образом, главным достоинством публикации является дифференцированный и комплексный подход к данной категории пациентов. На основании данных анамнеза, клиники, нейровизуализации и проведения ВЭМ в раннем послеоперационном периоде, авторы определяют группу пациентов с высоким риском развития эпилепсии, рекомендуя им длительную терапию, и группу с низким риском, оставляя ее без лечения, но под наблюдением. Такой подход позволяет избавить часть пациентов от необходимости необоснованного длительного приема антиэпилептических препаратов, которые являются потенциально токсичными.
Статья написана хорошим научным языком, является актуальной, обе пациентки обследованы современными методами, выводы адекватны. Авторами представлен обзор современной зарубежной литературы по данной тематике.
Единственное пожелание, касающееся этой работы, — проведение хотя бы минимального катамнестического наблюдения за пациентками.
К.Ю. Мухин (Москва)
Список литературы:
- Englot D, Chang E, Vecht C. Epilepsy and brain tumors. Handbook of clinical neurology 2016. https://doi.org/10.1016/b978-0-12-802997-8.00016-5
- Sirven J, Wingerchuk D, Drazkowski J, Lyons M, Zimmerman R. Seizure prophylaxis in patients with brain tumors: a metaanalysis. Mayo Clinic Proceedings: Elsevier BV. 2004;79(12):1489-1494. https://doi.org/10.4065/79.12.1489
- Мухин К.Ю. Эпилептические синдромы. Диагностика и терапия. Руководство для врачей. 2014.
- Chadwick D. Starting and stopping treatment for seizures and epilepsy. Epilepsia. Wiley-Blackwell. 2006 Oct;47(s1):58-61. https://doi.org/10.1111/j.1528-1167.2006.00662.x
- Glauser T, Ben-Menachem E, Bourgeois B, Cnaan A, Chadwick D, Guerreiro C, Kalviainen R, Mattson R, Perucca E, Tomson T. ILAE treatment guidelines: evidence-based analysis of antiepileptic drug efficacy and effectiveness as initial monotherapy for epileptic seizures and syndromes. Epilepsia. Wiley-Blackwell. 2006;47(7):1094-120. https://doi.org/10.1111/j.1528-1167.2006.00585.x
- The Causes of Epilepsy. Handbook of Epilepsy Treatment. Wiley-Blackwell; 2011 Mar 16;33-74. https://doi.org/10.1002/9781444325201.ch4
- Литовченко Т.А. Эпилепсия и эпилептические припадки после нейрохирургических операций. Украинский вестник психоневрологии. 2014;22(3).
- Tigaran S, Cascino GD, McClelland RL, So EL, Richard Marsh W. Acute postoperative seizures after frontal lobe cortical resection for intractable partial epilepsy. Epilepsia. Wiley-Blackwell; 2003 Jun 9;44(6):831-835. https://doi.org/10.1046/j.1528-1157.2003.56402.x
- Kombogiorgas D, Jatavallabhula NS, Sgouros S, Josan V, Walsh AR, Hockley AD. Risk factors for developing epilepsy after craniotomy in children. Child’s Nervous System Springer Nature. 2006 May 30;22(11):1441-1445. https://doi.org/10.1007/s00381-006-0117-4
- Upchurch K, Stern JM, Salamon N, Dewar S, Engel J, Vinters HV, et al. Epileptogenic temporal cavernous malformations: operative strategies and postoperative seizure outcomes. Seizure Elsevier BV. 2010 Mar;19(2):120-128. https://doi.org/10.1016/j.seizure.2009.11.006
- Manaka S, Ishijima B, Mayanagi Y. Postoperative seizures: epidemiology, pathology, and prophylaxis. Neurologia medico-chirurgica. Japan Neurosurgical Society. 2003;43(12):589-600. https://doi.org/10.2176/nmc.43.589
- Foy PM, Chadwick DW, Rajgopalan N, Johnson AL, Shaw MD. Do prophylactic anticonvulsant drugs alter the pattern of seizures after craniotomy? Journal of Neurology, Neurosurgery & Psychiatry. 1992 Sep 1;55(9):753-757. https://doi.org/10.1136/jnnp.55.9.753
- Siomin V, Angelov L, Li L, Vogelbaum MA. Results of a survey of neurosurgical practice patterns regarding the prophylactic use of anti-epilepsy drugs in patients with brain tumors. Journal of Neuro-Oncology. Springer Nature. 2005 Sep;74(2):211-215. https://doi.org/10.1007/s11060-004-6912-4
- Michelucci R. Optimizing therapy of seizures in neurosurgery. Neurology. Ovid Technologies (Wolters Kluwer Health). 2006 Dec 26;67(Issue 12, Supplement 4):S14-S18. https://doi.org/10.1212/wnl.67.12_suppl_4.s14
- Glantz MJ, Cole BF, Forsyth PA, Recht LD, Wen PY, Chamberlain MC, et al. Practice parameter: anticonvulsant prophylaxis in patients with newly diagnosed brain tumors: report of the quality standards subcommittee of the American Academy of Neurology. Neurology. Ovid Technologies (Wolters Kluwer Health). 2000 May 23;54(10):1886-1893. https://doi.org/10.1212/wnl.54.10.1886
- Forsyth PA, Weaver S, Fulton D, Brasher PMA, Sutherland G, Stewart D, et al. Prophylactic anticonvulsants in patients with brain tumour. Canadian Journal of Neurological Sciences/Journal Canadien des Sciences Neurologiques. Cambridge University Press (CUP). 2003 May;30(02):106-112. https://doi.org/10.1017/s0317167100053361
- Tremont-Lukats IW, Ratilal BO, Armstrong T, Gilbert MR. Antiepileptic drugs for preventing seizures in people with brain tumors. Tremont-Lukats IW, editor. Cochrane Database of Systematic Reviews: John Wiley & Sons Ltd. 2008 Apr 23. https://doi.org/10.1002/14651858.cd004424.pub2
- Varelas PN, Spanaki MV, Mirski MA. Seizures and the neurosurgical intensive care unit. Neurosurgery Clinics of North America: Elsevier BV. 2013 Jul;24(3):393-406. https://doi.org/10.1016/j.nec.2013.03.005
- Claassen J, Taccone FS, Horn P, Holtkamp M, Stocchetti N, Oddo M. Recommendations on the use of EEG monitoring in critically ill patients: consensus statement from the neurointensive care section of the ESICM. Intensive Care Medicine. Springer Nature. 2013 May 8;39(8):1337-1351. https://doi.org/10.1007/s00134-013-2938-4






