Абстракт
Введение
Абсолютными показаниями для начала ИВЛ у нейрохирургических пациентов являются: коматозное состояние, эпилептический статус, гипоксемия, гиперкапния или гипокапния. В клинической практике нередко ИВЛ начинается до формирования абсолютных показаний на основании экспертной оценки лечащих врачей. Для объективизации показаний к ИВЛ была создана шкала оценки тяжести дыхательной недостаточности (ДН). Шкала состоит из трех блоков, оценивающих уровень сознания, выраженность нарушений глотания, кашля, проходимости дыхательных путей и степень паренхиматозного повреждения легких. По созданной шкале 4 и более баллов является показанием к ИВЛ. Разработанная шкала была апробирована в клинических условиях.
Материалы и методы
Апробация шкалы проводилась в период с декабря 2009 по март 2010 года. При тотальной выборке пациентов в соответствии с выбранными критериями включения и исключения в исследование вошло 15 пациентов. Из них было 8 женщин (53%) и 7 мужчин (47%). Возраст пациентов 25 – 68 лет, медиана 42 года. В 7 наблюдениях были аневризмы сосудов головного мозга, у 8 пациентов – опухоли головного мозга различной локализации и гистологии. Эти пациенты оценивались по шкале, но показания к ИВЛ определяли лечащие врачи, не владевщие шкалой.
Результаты
Было выделено 3 группы. Первые две группы – это пациенты с успешной экстубацией, но пациенты второй группы были реинтубированы отсроченно в связи с ухудшением неврологической симптоматики. У пациентов третьей группы экстубация была неуспешной, то есть они потребовали реинтубации в течение 48 часов после экстубации. У пациентов 2 и 3 групп развивались воспалительные осложнения - нозокомиальная пневмония и сепсис, были хуже исходы. Если бы тактика в отношении начала ИВЛ определялась оценкой по шкале, то она не отличалась бы в 1 и 2 группах. У пациентов 3 группы, исходя из шкальной оценки, ИВЛ должна была бы возлбновляться гораздо раньше, чем это осуществлялось на практике.
Выводы
Созданная шкала позволяет оптимизировать сроки начала ИВЛ. Однократная оценка пациента позволяет установить непосредственную причину ДН, а динамическая оценка - определить последовательность изменения выраженности отдельных факторов, определяющих ДН. У пациентов с неуспешной экстубацией трахеи шкала позволит оптимизировать сроки реинтубации и, в результате, снизить частоту развития нозокомиальной и аспирационной пневмонии
Введение
По данным современной литературы, абсолютными показаниями к началу ИВЛ являются [2,3,10,19,28,31]:
- Остановка сердечной деятельности;
- Апноэ или брадипноэ менее 8 дыханий в минуту, тахипноэ более 35 дыханий в минуту;
- Коматозное состояние;
- Эпилептический статус, требующий введения седативных препаратов;
- Прогрессирующая гипоксемия, рефрактерная к кислородотерапии (РаО2 < 60 мм рт.ст, SaO2 < 90 %, рО2/FiО2<200);
- Гиперкапния РаСО2 > 55 мм рт.ст. (у больных ХОЗЛ РаСО2 > 65 мм рт.ст.) и гипокапния РаСО2 < 30 мм рт.ст.
Специфическими причинами дыхательной недостаточности (ДН) у нейрохирургических пациентов являются повреждения ЦНС, приводящие к нарушению функции дыхательной мускулатуры или гортаноглотки [5,9,20]. В первом случае нарушается глубина, частота и ритм дыхания, а во втором возникает нарушение проходимости дыхательных путей и угроза аспирации.
Острое повреждение головного мозга приводит к нарушению механизмов центральной регуляции дыхания, что вызывает ДН. В этих условиях стремительно формируется порочный круг: гипоксия усугубляет повреждение ЦНС, в результате чего углубляется дыхательная недостаточность и гипоксия. В соответствии с международными рекомендациями по лечению пациентов с травматическим повреждением головного мозга, уровень сознания по шкале комы Глазго (ШКГ) < 9 баллов является показанием для начала ИВЛ. Фактически это профилактическая ИВЛ, которая позволяет предотвратить развитие гипоксии [6,7,8].
В настоящее время решение о начале ИВЛ у нейрохирургических пациентов при отсутствии абсолютных показаний принимается на основе экспертного мнения лечащего врача [27]. Нередко аргументация в пользу или против ИВЛ при отсутствии чётких критериев носит эмоциональный характер. Сложность определения показаний для начала ИВЛ не в том, что угнетение сознания, нарушения функций ствола мозга (дыхательный центр, глотание и проходимость дыхательных путей) и заболевания органов дыхания per se могут по отдельности приводить к ДН. Наибольшая трудность возникает, когда каждый из перечисленных факторов не является критическим, но сочетание нескольких патологических процессов определяют тяжесть состояния пациента.
Опираясь на наш опыт, была создана многофакторная шкала для оценки ДН. Главная цель созданной шкалы – это раннее выявление ДН, своевременное начало ИВЛ и предотвращение формирования вторичных повреждений мозга. Также нами была проведена оценка эффективности созданной шкалы.
Материалы и методы
Работа состояла из двух этапов: ретроспективного и проспективного. На первом этапе мы на основании нашего опыта разработали шкалу тяжести ДН у нейрохирургических пациентов (Таблица 1). В Институте ежегодно выполняется около 6000 нейрохирургических операций, 2700 – 3000 пациентов поступает в отделение реанимации и интенсивной терапии, 450 – 500 пациентов пребывает в нашем отделении более 48 часов. Мы считаем допустимым создание шкалы на основывании опыта одного отделения, поскольку такие шкалы, как MODS и SOFA, составленные для оценки тяжести полиорганной дисфункции, были разработаны только на основании обзора литературы и консенсуса экспертов [4,25,34].
Таблица 1
Шкала оценки тяжести дыхательной недостаточности у нейрохирургических пациентов.
| 0 баллов | 1 балл | 2 балла | 3 балла | 4 балла | |
| Возбуждение и седация - оценка по шкале RASS Угнетение сознания (сомноленция; оглушение, сопор, кома)1 | По RASS 0: Спокойствие и внимательность (ясное сознание) | По RASS -1/+1: Беспокойст-во/ сонлив-ость (сомнолен-ция). | По RASS -2/+2: Ажитация /Легкая седация (оглушение). | По RASS -3-4/+3+4: Выраженная ажитация с агрессией; Умеренная или лубокая седация (сопор). | По RASS -5: Отсутствие пробуждения (кома) |
| Нарушения глотания, кашля, проходимости дыхательных путей. | Глотание сохранено. Кашель эффективный. Проходимость дыхательных путей сохранена. | Глотание сохранено. Кашель не эффективный. Проходимость дыхательных путей сохранена. | Глотание нарушено. Кашель эффективный. Проходимость дыхательных путей сохранена. | Глотание нарушено. Кашель не эффективный. Проходимость дыхательных путей сохранена. | Глотание нарушено. Кашель не эффективный. Проходимость дыхательных путей нарушена. |
| Индекс pO2/FiO2 | >300 | 250-300 | 220-250 | 200-220 | <200 |
При ожирении пациента (индекс массы тела > 30) общая сумма баллов увеличивается на 1 балл.
1 - RASS – Richmond assessment - Richmond Agitation Sedation Scale – Ричмондская шкала оценки ажитации и седации.
Шкала создана для прикроватной оценки тяжести ДН и принятия решения о необходимости начала ИВЛ. Шкала состоит из трех блоков.
- Оценка уровня сознания
- Оценка нарушения глотания, кашля и проходимости дыхательных путей
- Индекс pO2/FiO2
Первый блок включает в себя оценку нарушений сознания. Для оценки степени психомоторного возбуждения и уровня седации мы использовали шкалу RASS (Ричмондская шкала оценки ажитации и седации), которая специально была создана для этих целей 15.
Таблица 2
RASS: Ричмондская шкала оценки ажитации и седации.
| +4 | Пациент агрессивен | Пациент агрессивен, возникают эпизоды выраженного психомоторного возбуждения, возможно нанесение физического ущерба медицинскому персоналу |
| +3 | Выраженная ажитация | Пациент агрессивен, удаляет катетеры, зонды, дренажи, трубки |
| +2 | Ажитация | Частая нецеленаправленная двигательная активность, «борьба» с респиратором при проведении ИВЛ |
| +1 | Беспокойство | Пациент беспокоен, иногда испуган, но неагрессивен, а двигательная активность не имеет деструктивной направленности |
| 0 | Спокойствие и внимательность | |
| -1 | Сонливость | Не достаточно внимателен, пробуждается на оклик отсроченно: открывает глаза, фиксирует взор более 10 секунд |
| -2 | Легкая седация | Пробудим на оклик (открывает глаза, но фиксирует взор менее 10 секунд) |
| -3 | Умеренная седация | Двигательная активность или открывание глаз в ответ на оклик без фиксации взора |
| -4 | Глубокая седация | Нет реакции на оклик, но двигательная активность или открывание глаз на проприоцептивные и ноцицептивные раздражители |
| -5 | Отсутствие пробуждения | Нет реакции ни на оклик, ни на проприоцептивные и ноцицептивные раздражители |
Для оценки уровня угнетения сознания мы использовали критерии, описанные в литературе [35]:
- Сомноленция: пациент сонлив, но легко разбудим. Продолжительность сна увеличиена, но фазность сон – бодрствование сохранена (1 балл).
- Оглушение: пациент заторможен, сонлив, апатичен, выполняет инструкции и отвечает на вопросы с задержкой (2 балла).
- Сопор: пациент может выполнить простые инструкции только после повторных и интенсивных обращений. Вербальный контакт в виде односложных ответов может быть как сохранен, так и отсутствовать. Вне обращения у пациента вновь происходит угнетение сознания. Двигательный ответ часто носит стереотипный характер, иногда развивается стереотипное двигательное беспокойство (3 балла).
- Кома: пациент на вопросы не отвечает, инструкций не выполняет, спонтанного открывания глаз нет, движения отсутствуют или носят патологический характер (4 балла).
Ясное сознание оценивается по первому блоку нашей шкалы в 0 баллов, RASS +1/-1 и сомноленция – в 1 балл, RASS +2/-2 и оглушение – в 2 балла, RASS +3,+4/-3,-4 и сопор - в 3 балла, кома – в 4 балла (Таблица 1). Коматозное состояние является показанием для начала ИВЛ.
Второй блок содержит в себе критерии оценки нарушений глотания, кашля и проходимости дыхательных путей. Оценка критериев выполняется в упрощённом виде по принципу нарушен/сохранен:
- Оценка глотания: Глотание нарушено, если в ротоглотке выявляется скопление слюны, которую пациент не в состоянии проглотить; или если при попытке проглотить тестовый болюс в виде 5 мл жидкости есть признаки аспирации (пациент поперхивается или после глотка возникают влажные хрипы).
- Оценка кашля: Эффективным считается звучный или звонкий кашель с хорошим изгнанием мокроты из верхних отделов трахеи и гортани. Сиплый или глухой кашель, сопровождающийся хриплым дыханием и невозможностью изгнать мокроту из верхних отделов трахеи и гортани, считается неэффективным.
- Оценка проходимости верхних дыхательных путей (ВДП): Во всех случаях, когда при дыхании наблюдается стридорозный компонент в виде затрудненного вдоха, шумов или хрипов на вдохе и включение дополнительной дыхательной мускулатуры, – проходимость ВДП нарушена.
При наличии сохранного глотания, кашля и проходимости дыхательных путей эти нарушения оценивается по второму блоку нашей шкалы в 0 баллов, при сохранном глотании и нарушенном кашле – в 1 балл, при нарушеном глотании и сохраненном кашле - в 2 балла, при нарушении глотания и кашель - в 3 балла (Таблица 1). При нарушениях глотания и/или отсутствии кашля во всех случаях устанавливался назогастральный зонд, через который проводилось энтеральное кормление. Если у пациента нарушена проходимость дыхательных путей, то по второму блоку созданной нами шкалы нарушения оцениваются в 4 балла (Таблица 1), и пациенту показана незамедлительная интубация трахеи и возобновление ИВЛ.
Особую группу составляют пациенты, набравшие 4 балла только за счет второго блока шкалы (нарушнений глотания, кашля и проходимости дыхательных путей), но не имеющие нарушений сознания, снижения индекса рО2/FiО2 и изменения механики дыхания. Такие пациенты могут быть переведены на спонтанное дыхание после обеспечения надёжной проходимости дыхательных путей и защиты от аспирации (трахеостомия с использованием трубки с герметизирующей манжеткой). Для выделения этой группы с 2006 года в Институте успешно применяется шкала бульбарных нарушений [1]. Этим пациентам выполняется трахеостомия, после чего они проходят реабилитацию на спонтанном дыхании с использованием трахеостомических трубок с герметизирующими манжетками.
Третий блок шкалы учитывает выраженность паренхиматозного повреждения легких. Для этого мы измеряли индекс рО2/FiО2. Если индекс рО2/FiО2 более 300, то повреждение легких оценивается в 0 баллов, если индекс 250-300, то - в 1 балл, если индекс 220-250, то - в 2 балла, если индекс 200-220, то - в 3 балла, если индекс менее 200, то - в 4 балла (Таблица 1). Индекс рО2/FiО2 менее 200 указывает на выраженную ДН, при которой необходимо экстренно начинать ИВЛ.
Шкала составлена таким образом, что каждый из 3 блоков начинается критериями нормы: ясное сознание, сохраненные глотание, кашель и проходимость дыхательных путей, индекс рО2/FiО2 более 300. Здоровый человек по этой шкале будет иметь 0 баллов. Заканчиваются блоки критериями, характеризующими крайнюю выраженность патологического состояния: коматозное состояние или глубокая седация, отсутствие проходимости дыхательных путей и индекс рО2/FiО2 менее 200. Изолированно каждое из этих состояний является абсолютным показанием для начала ИВЛ [2,3,10,19,28,31]. Однако между нормой и абсолютными показаниями для начала ИВЛ существует множество промежуточных клинических состояний, когда у пациента развивается сочетание различной выраженности нарушений сознания, глотания, кашля, проходимости дыхательных путей и паренхиматозного повреждения легких. У таких пациентов показания для начала ИВЛ устанавливаются лечащим доктором на основании его личного опыта. Созданная нами шкала разработана для объективизации показаний к началу ИВЛ. Так, если пациент имеет суммарную оценку по шкале 4 и более баллов, то он нуждается в проведении ИВЛ. При ожирении пациента ухудшается функция дыхания [18], поэтому при индексе массы тела более 30 общая сумма баллов по шкальной оценке увеличивается на 1 балл.
Шкала оценки тяжести ДН у нейрохирургических больных создана для динамической оценки выраженности ДН у этих пациентов, последовательности развития нарушения сознания, глотания, кашля, проходимости дыхательных путей и паренхиматозного повреждения легких, а также для возможности оценки эффективности проводимой терапии
Целью второго, проспективного, этапа проведенного исследования явилась апробация созданной шкалы. Этот этап соответствовал критериям обсервационного исследования. Набор пациентов производился в период с декабря 2009 года по март 2010 года в соответствии с критериями включения и исключения пациентов. Критериями включения были:
- Возраст старше 18 лет;
- Нейрохирургические пациенты, находящиеся на самостоятельном дыхании;
- Оценка состояния больных по созданной нами шкале более 1 балла: беспокойство/сомноленция или неэффективный кашель с нормальным глотанием и сохранной проходимостью дыхательных путей или индекс рО2/FiО2 250-300.
Критериями исключения были:
Абсолютные показания для интубации трахеи и начала ИВЛ - коматозное состояние; - pO2<60 мм.рт.ст., pCO2<30 мм.рт.ст. и >50 мм.рт.ст., pO2/FiO2<200; - нарушение проходимости верхних дыхательных путей.
Внутричерепная гипертензия; Острая нейрохирургическая патология, требующая экстренных хирургических вмешательств (интракраниальная гематома, окклюзионная гидроцефалия и т.д.).
За этот период при тотальной выборке среди пациентов, поступивших после операций в отделение реанимации, было выявлено 15 пациентов, удовлетворявших вышеуказанным критериям. Из них было 8 женщин (53%) и 7 мужчин (47%). Возраст пациентов 25 – 68 лет, медиана 42 года. В 7 наблюдениях были аневризмы сосудов головного мозга, у 8 пациентов – опухоли головного мозга различной локализации и гистологии (Таблица 3). Длительность ИВЛ после операции до первой экстубации составила от 4 до 192 часов, медиана 18 часов. После операции все пациенты были экстубированы. Критериями готовности к экстубации были:
- Восстановление бодрствования, сознания, глоточного, кашлевого рефлексов;
- Успешное прохождение теста спонтанного дыхания в течение часа (SBT (spontaneous breathing trial));
- pO2>60 мм.рт.ст, pCO2 30 – 50 мм.рт.ст, индекс рО2/FiО2>200.
После прекращения респираторной поддержки все эти пациенты были оценены лечащими врачами как «пациенты, требующие наблюдения в отделении реанимации и/или проведения интенсивной терапии». По газовому составу артериальной крови все пациенты после экстубации были компенсированы: pO2>60 мм.рт.ст, pCO2 30–50 мм.рт.ст, индекс рО2/FiО2>200.
Оценка по созданной шкале всех включенных в исследование пациентов после экстубации была более 1 балла (Таблица 3). При помощи КТ-исследования головного мозга была исключена нейрохирургическая патология, требующая экстренных вмешательств. Решения о реинтубации и возобновлении ИВЛ принимались лечащими врачами отделения, которые не участвовали в создании этой шкалы и которые не знали результатов балльной оценки состояния пациентов. Это позволило минимизировать влияние получаемых результатов оценки пациентов по созданной шкале на определение дальнейшей терапевтической тактики. Оценка по шкале производилась каждые 6 часов и каждый раз при ухудшении состояния. Однако для облегчения восприятия материала в таблицах 3,4 приведена сумма баллов приведена на этапах изменения лечебной тактики. Значение А: при пролонгировании наблюдения пациента в отделении реанимации в связи с нестабильным состоянием (оценка по шкале > 1 балла), но при отсутствии абсолютных показаний для экстренной реинтубации и возобновления ИВЛ; значение В – перед реинтубацией в случае развития абсолютных показаний или экспертного мнения лечащего доктора при отсутствии абсолютных показаний для начала ИВЛ; или при переводе пациента из отделения реанимации в нейрохирургическое отделение; значение С (у пациентов с реинтубацией) – после повторной экстубации; значение D – перед повторной реинтубацией или при переводе в нейрохирургическое отделение.
Таблица 3
Характеристика проспективной группы: демографические данные, диагноз, количество экстубаций и реинтубаций, длительность ИВЛ, осложнения и исходы.
- Возраст
- Пол
- Кол-во экстубаций
- Кол-во интубаций в ОРИТ
- Длительность ИВЛ через интуба-ционную трубку после операции
- Длительность спонтанного дыхания в ОРИТ после 1ой экстубации
- Длительность ИВЛ через интубационную трубку после 1ой реинтубации
- Длительность спонтанного дыхания в ОРИТ после 2ой экстубации
- Длительность ИВЛ через интубационную трубку после 2ой реинубации
- Длительность ИВЛ через трахеостомическую трубку
- Длительность самосто-ятельного дыхания через трахеостомическую трубку в ОРИТ
- Длительность канюленосительства
- Динамика балльной оценки по шкале 1
- Осложнения и примечания
| 1 | 2 | Диагноз | Операция | 3 | 4 | 5 | 6 | 7 | 8 | 9 | Результат: самостоятельное дыхание или трахео-стомия | 10 | 11 | 12 | 13 | 14 | Исход | |
| 1 | 30 | Ж | Нейроцитома боковых желудочков. | Удаление опухоли. | 1 | 1 | 18 ч. | 5 сут | 2 сут | - | - | Трахео-стомия на 6 сут п/о | 54 сут | - | - | 3 – 8 (А – B) | Менинго-энцефалит | Летальный исход на 62 сут п/о (ШИГ-1) |
| 2 | 58 | Ж | Глиобластома моста. | Открытая биопсия опухоли. | 1 | 1 | 16 ч. | 5 ч. | 2 сут | - | - | Трахео-стомия на 3 сут п/о | 37 сут | - | - | 5 – 7 (A – B) | Пневмония. Продолжен-ный рост опухоли | Летальный исход на 39 сут п/о (ШИГ-1) |
| 3 | 48 | М | Хориоидпа-пиллома IV желудочка | Удаление опухоли | 1 | 0 | 4 ч. | 4 сут | - | - | - | Самосто-ятельное дыхание | - | - | - | 3 – 2 (A – B) | Массивная интраопе-рационная воздушная эмболия | Из ОРИТ переведен на 4 сут п/о, из Института выписан на 19 сут п/о (ШИГ-5) |
| 4 | 68 | Ж | Глиобластома левой лобно-височной области | Удаление опухоли | 2 | 1 | 22 ч. | 12 ч. | 3 сут | 1 сут | - | Самосто-ятельное дыхание | - | - | - | 5 - 8 – 2 (A – B – C) | - | Из ОРИТ переведен на 5 сут п/о, из Института выписан на 11 сут п/о (ШИГ-4) |
| 5 | 51 | М | Аневризма левой СМА, правой СМА. | Клипиро-вание аневризм | 1 | 0 | 5 ч. | 7 сут | - | - | - | Самосто-ятельное дыхание | - | - | - | 3 – 1 (A – B) | - | Из ОРИТ переведен на 7 сут п/о, из Института выписан на17 сут п/о (ШИГ-4) |
| 6 | 61 | М | Аневризма ПМА-ПСА справа | Клипиро-вание аневризмы | 1 | 0 | 9 ч. | 1 сут | - | - | - | Самосто-ятельное дыхание | - | - | - | 3 – 2 (A – B) | Преморбид: ХОБЛ | Из ОРИТ переведен на 2 сут п/о, из Института выписан на 28 сут п/о (ШИГ-5) |
| 7 | 42 | М | Аневризма ПМА-ПСА слева | Окклюзия аневризмы микроспи-ралями | 1 | 0 | 15 ч. | 4 сут | - | - | - | Самосто-ятельное дыхание | - | - | - | 3 – 1 (A – B) | - | Из ОРИТ переведен на 5 сут п/о, из Института выписан на 19 сут п/о (ШИГ-5) |
| 8 | 30 | Ж | Экстравен-трикулярная краниио-фарингиома | Удаление опухоли | 1 | 0 | 3 ч. | 14 сут | - | - | - | Самосто-ятельное дыхание | - | - | - | 3 – 2 (A – B) | Гипопитуи-таризм. Водно-электролит-ные наруш. | Из ОРИТ переведен на 14 сут п/о, из Института выписан на 24 сут п/о (ШИГ-4) |
| 9 | 58 | М | Аневризма ЗМА слева | Окклюзия аневризмы микроспи-ралями | 1 | 0 | 96 ч. | 10 сут | - | - | - | Самосто-ятельное дыхание | - | - | - | 3 – 2 (A – B) | Менинго-энцефалит | Из ОРИТ переведен на 14 сут п/о, из Института выписан на 29 сут п/о (ШИГ-4) |
| 10 | 25 | Ж | Интра-экстравен-трикулярная краниио-фарингиома | Удаление опухоли | 1 | 1 | 5 ч. | 7 сут | 2 сут | - | - | Трахео-стомия на 9 сут п/о | 26 сут | 4 сут | 47 сут | 3 – 9 (A – B) | Гипопитуи-таризм. Пневмония | Из ОРИТ переведен на 39 сут п/о, из Института выписан на 78 сут п/о (ШИГ-3) |
| 11 | 40 | Ж | Петрокливаль-ная менингио-ма справа | Удаление опухоли | 2 | 1 | 18 ч. | 5 ч. | 1 сут | 7 сут | - | Самосто-ятельное дыхание | - | - | - | 4 – 6 – 3 (A – B – C) | - | Из ОРИТ переведен на 9 сут п/о, из Института выписан на 18 сут п/о (ШИГ-4) |
| 12 | 31 | М | Аневризма ПМА-ПСА справа | Клипиро-вание аневризмы | 2 | 2 | 192 ч. | 3 ч. | 6 сут | 1,5 ч. | 2 сут | Трахео-стомия на 16 сут п/о | 36 сут | 15 сут | 53 сут | 4 – 6 – 5 – 7 (A – B – C – D) | Пневмония. Сепсис. | Из ОРИТ переведен на 51 сут п/о, из Института выписан на 65 сут п/о (ШИГ-3) |
| 13 | 41 | Ж | Аневризма СМА справа, ВСА слева | Клипиро-вание аневризмы ВСА слева | 1 | 0 | 168 ч. | 2 сут | - | - | - | Самосто-ятельное дыхание | - | - | - | 2 – 1 (A – B) | - | Из ОРИТ переведен на 9 сут п/о, из Института выписан на 17 сут п/о (ШИГ-4) |
| 14 | 46 | М | Аневризма ПМА-ПСА справа | Клипиро-вание аневризмы | 2 | 2 | 72 ч. | 1 сут | 4 сут | 2 сут | 2 ч. | Трахео-стомия на 10 сут п/о | 11 сут | 3 | 24 | 10 – 10 – 8 – 10 (A – B – C – D) | Пневмония | Из ОРИТ переведен на 33 сут п/о, из Института выписан на 53 сут п/о (ШИГ-3) |
| 15 | 29 | Ж | Нейрофибро-матоз II типа, 2-сторонние невриномы VIII нервов | Удаление невриномы VIII нерва слева. | 1 | 0 | 144 ч. | 6 сут | - | - | - | Самостоятельное дыхание | - | - | - | 3 – 3 (A – B) | - | Из ОРИТ переведен на 12 сут п/о, из Института выписан на 22 сут п/о (ШИГ-3) |
Примечания. 1 – Приведена сумма баллов по шкале. Оценка производилась в динамике несколько раз. Значение А: сумма баллов при пролонгировании наблюдения пациента в отделении реанимации в связи с нестабильным состоянием (оценка по шкале > 1 балла), но при отсутствии абсолютных показаний для экстренной реинтубации и возобновления ИВЛ; Значение В – перед реинтубацией в случае развития абсолютных показаний или экспертного мнения лечащего доктора при отсутствии абсолютных показаний для начала ИВЛ; или при переводе пациента из отделения реанимации в нейрохирургическое отделение; Значение С (у пациентов с реинтубацией) – после повторной экстубации; Значение D – перед повторной реинтубацией или при переводе в нейрохирургическое отделение.
П/о – после операции. ПМА – передняя мозговая артерия. ПСА – передняя соединительная артерия. ЗМА – задняя мозговая артерия.
ХОБЛ – хроническая обструктивная болезнь легких.
Таблица 4
Динамика балльной оценки пациентов по шкале тяжести дыхательной недостаточности.
| Пациенты | Оценка тяжести ДН в динамике. | Нарушения глотания | Индекс рО2/FiО2 | Шкала RASS | Ожирение | Общая оценка |
| 1 | A | 2 | 0 | 1 | 0 | 3 |
| B | 3 | 2 | 3 | 0 | 8 | |
| 2 | A | 2 | 1 | 1 | 1 | 5 |
| B | 3 | 2 | 1 | 1 | 7 | |
| 3 | A | 0 | 3 | 0 | 0 | 3 |
| B | 0 | 2 | 0 | 0 | 2 | |
| 4 | A | 2 | 2 | 1 | 0 | 5 |
| B | 2 | 3 | 3 | 0 | 8 | |
| C | 2 | 0 | 0 | 0 | 2 | |
| 5 | A | 0 | 2 | 1 | 0 | 3 |
| B | 0 | 0 | 1 | 0 | 1 | |
| 6 | A | 0 | 2 | 0 | 1 | 3 |
| B | 0 | 1 | 0 | 1 | 2 | |
| 7 | A | 0 | 1 | 2 | 0 | 3 |
| B | 0 | 1 | 0 | 0 | 1 | |
| 8 | A | 0 | 1 | 2 | 0 | 3 |
| B | 0 | 0 | 2 | 0 | 2 | |
| 9 | A | 0 | 2 | 1 | 0 | 3 |
| B | 0 | 1 | 1 | 0 | 2 | |
| 10 | A | 0 | 1 | 2 | 0 | 3 |
| B | 3 | 3 | 3 | 0 | 9 | |
| 11 | A | 3 | 1 | 0 | 0 | 4 |
| B | 3 | 1 | 2 | 0 | 6 | |
| C | 2 | 1 | 0 | 0 | 3 | |
| 12 | A | 0 | 3 | 1 | 0 | 4 |
| B | 0 | 4 | 2 | 0 | 6 | |
| C | 0 | 3 | 2 | 0 | 5 | |
| D | 0 | 4 | 3 | 0 | 7 | |
| 13 | A | 0 | 0 | 2 | 0 | 2 |
| B | 0 | 0 | 1 | 0 | 1 | |
| 14 | A | 3 | 4 | 3 | 0 | 10 |
| B | 3 | 4 | 3 | 0 | 10 | |
| C | 3 | 2 | 3 | 0 | 8 | |
| D | 3 | 4 | 3 | 0 | 10 | |
| 15 | A | 3 | 0 | 0 | 0 | 3 |
| B | 3 | 0 | 0 | 0 | 3 |
Результаты исследования и их обсуждение
Во время второго, проспективного, этапа исследования была апробирована созданная шкала. В результате было выделено 3 группы пациентов. В I и II группах экстубация была успешной (10 больных – 67%), в III группе - неуспешной (5 больных – 33%) (Рисунок 1).
Рисунок 1.
Распределение пациентов на втором, проспективном, этапе исследования.
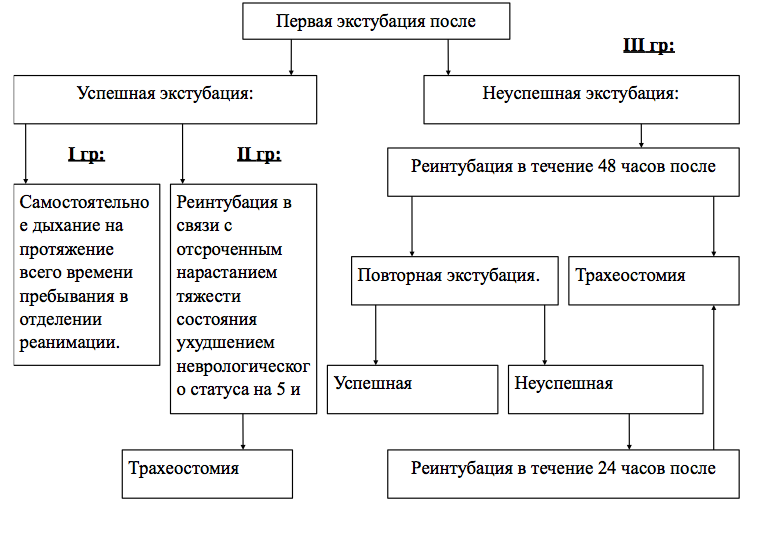
По литературным данным, экстубация является успешной, если самостоятельное дыхание продолжается в течение 24 - 72 часов [17,26]. По нашему опыту, для описания успешности экстубации у нейрохирургических пациентов целесообразно использовать временной промежуток в 48 часов. У пациентов с поврежденным мозгом наиболее трудно прогнозировать успешность экстубации [12].
I группа
Эту группу составили 8 пациентов (53%), которые были успешно экстубированы после операции и затем дышали самостоятельно на протяжении всего последующего времени пребывания в отделении реанимации (наблюдения: 3,5,6,7,8,9,13,15). При оценке этих пациентов по шкале на протяжении всего времени пребывания в отделении реанимации сумма баллов не превышала 3 (Табл. 3,4). У пациентов этой группы не отмечалось одновременного изменения сознания, снижения индекса рО2/FiО2 и нарушения глотания, кашля, проходимости дыхательных путей. Тяжесть ДН в этой группе была обусловлена одной (наблюдения: 3,6,13,15), или максимум двумя (наблюдения: 5,7,8,9) составляющими созданной шкалы. Индекс рО2/FiО2 определял тяжесть у 6 пациентов (наблюдения 3,5,6,7,8,9), изменение уровня сознания - у 5 пациентов (наблюдение 5,7,8,9,13), бульбарные нарушения – у одной пациентки (наблюдение 15). Не было ни одного наблюдения, когда лечащий врач принимал бы решение о реинтубации трахеи и возобновлении ИВЛ у пациента с суммой баллов по шкале 3 и менее баллов.
Пациенты I группы находились в отделении реанимации в течение 8,4±4,6 суток (m±sd), у них не развивалось пневмонии. По шкале исходов Глазго (ШИГ) при выписке из Института 5 баллов было у трех пациентов (наблюдения 3,6,7), 4 балла – у 4 пациентов (наблюдения 5,8,9,13) и 3 балла – в наблюдении 15.
Таким образом, пациенты, у которых в течение всего времени пребывания в отделении реанимации сумма баллов по созданной шкале не превышает 3 баллов, не нуждаются в реинтубации трахеи и возобновлении ИВЛ и имеют благопрятные исходы. Тяжесть ДН у них определяется преимущественно изменением уровня сознания и снижением индекса рО2/FiО2. У подавляющего большинства этих пациентов не выявлялось нарушений глотания, кашля, проходимости дыхательных путей.
Наиболее тяжелым наблюдением этой группы было 15 наблюдение.
Пациентка Б, 29 лет, поступила в Институт с диагнозом: Нейрофиброматоз II типа, двусторонние невриномы слуховых нервов и состояние после удаления опухолей в 2003, 2004, 2009 годах. До операции пациентка была в ясном сознании. Выявлялась глухота с двух сторон, онемение лица и снижение роговичных рефлексов с двух сторон, парез лицевого нерва, больше справа, множественный нистагм и шаткость походки, бульбарные нарушения. Сопутствующей соматической патологии выявлено не было. Во время операции произведено удаление невриномы VIII нерва слева без осложнений. В связи с нарастанием стволовой симптоматики в виде отсутствия глоточного и угнетения кашлевого рефлексов (нет реакции на интубационную трубку) ИВЛ проводилась в течение последующих 6 суток. Обращало на себя внимание отсутствие скопления слюны в полости рта. Затем пациентка была удачно экстубирована. Она не могла проглотить тестовый болюс в виде 5 мл воды, у нее не было кашля (3 балла по шкале), но в полости рта не было скопления слюны, то есть пациентка сглатывала слюну. Мы предполагаем, что это связано с развитием компенсаторных механизмов защиты верхних дыхательных путей у пациентов с длительно существующим воздействием на бульбарную группу черепно-мозговых нервов. Кроме этого, у пациентки не было паренхиматозного повреждения легких, и выявлялся высокий уровень бодрствования, адекватное сотрудничество с медицинским персоналом.
Пациентка оставалась в отделении реанимации в течение 6 суток для интенсивного наблюдения за ней. На 22 сутки после операции она была выписана из Института в ясном сознании, без двигательного дефицита, но требовала постоянного ухода за собой в связи с общей тяжестью своего состояния.
II группа
Эту группу составили два пациента. Они были успешно экстубированы, но в дальнейшем, на 5 – 7 сутки, потребовали возобновления ИВЛ (наблюдения 1,10). Причина заключалась в ухудшении состояния, стремительном угнетении сознания до сопора и нарастании бульбарных нарушений. Оба пациента были трахеостомированы. Сумма баллов до ухудшения состояния составляла 3 балла (Таблица 3,4). Тяжесть ДН в этих наблюдениях была обусловлена двумя составляющими шкалы (Таблица 4). Из этого следует, что эти пациенты до ухудшения их состояния находились на грани компенсации своих дыхательных функций. При стремительном ухудшении состояния сумма баллов по шкале быстро достигла 8 и 9 баллов, соответственно. На этом этапе лечащие врачи незамедлительно возобновляли ИВЛ.
Пациенты II группы находились в отделении реанимации в течение 62 и 78 суток. В наблюдении 10 развилась пневмония вследствие аспирации, произошедшей во время ухудшения состояния. По шкале исходов Глазго (ШИГ) она при выписке имела 3 балла В наблюдении 1 пациентка скончалась на фоне менингоэнцефалита (Таблица 3).
Пациентка С (наблюдение 10), 25 лет, поступила в Институт с диагнозом интра-экстра-вентрикулярная краниофарингиома. При поступлении выявлялся хиазмальный синдром и гипопитуитаризм. Через 5 часов после операции пациентка была экстубирована. Она оставалась в сознании, повторялись эпизоды психомоторного возбуждения, требовавшие использования седативных препаратов. Выявлялись гормональные и гомеостатические нарушения, которые удавалось корригировать методами интенсивной терапии. По нашей шкале суммарная оценка составила 3 балла – RASS +2/-2 и индекс рО2/FiО2=272. Состояние оставалось стабильным в течение последующих 6 суток. На 7 сутки состояние ухудшилось. Развилось сопорозное состояние, появились нарушения глотания и кашля, возникла аспирация, приведшая к снижению индекса рО2/FiО2. Оценка по шкале составила 9 баллов. Пациентка была незамедлительно реинтубирована и на 2 сутки трахеостомирована. Ухудшение состояния было связано с ишемическим повреждением диэнцефальной области, поскольку ведущим при ухудшении был диэнцефальный синдром. На фоне проводимой интенсивной терапии состояние было стабилизирована. Пациентка была переведена из отделения реанимации на 39 сутки, деканулирована – на 47 сутки после трахеостомии, а ваписана из Института – на 78 сутки после операции. По ШИГ у пациентки было 3 балла.
III группа
Эту группу составили 5 пациентов (33%) (наблюдения 2,4,11,12,14). Это пациенты с неуспешной экстубацией, то есть те наблюдения, в которых реинтубация и возобновление ИВЛ были произведены в течение 48 часов после экстубации. У всех пациентов этой группы сразу после экстубации сумма баллов по нашей шкале составила 4 и более баллов. В отличие от пациентов, которые не требовали начала ИВЛ во время нахождения в отделении реанимации, у этих пациентов тяжесть была обусловлена двумя (наблюдения 11,12) или тремя (наблюдения 2,4,14) составляющими нашей шкалы. У 4 из 5 пациентов выявлялись нарушения глотания и кашля. Это говорит о том, что эти нарушения являются более тяжелыми и, вероятно, прогностически более неблагоприятными, чем изменения уровня сознания и снижение индекс рО2/FiО2 [11,14,21,22,23,24,29,30,32,33]. Однако лечащими врачами осуществлялась выжидательная тактика. В результате до реинтубации пациенты дышали самостоятельно в течение 9,8±8,6 часов (Таблица 3).
4 пациентов были экстубированы во второй раз (наблюдения: 4,11,12,14). Успешной была повторная экстубация у двух пациентов (наблюдения 4,11). В этих наблюдениях суммарная оценка по шкале составила 2 и 3 балла, соответственно. Пациенты были переведены в нейрохирургическое отделение на самостоятельном дыхании. У оставшихся двух пациентов и повторная экстубация оказалась неуспешной (наблюдения 12,14). При этом оценка по шкале составила 5 и 8 баллов, соответственно. Первый пациент был реинтубирован через 1,5 часа после экстубации, а второй – через 48 часов. Оба эти пациента были трахеостомированы.
Длительность нахождения в отделении реанимации пациентов III группы составила 30,6±25,1 суток (m±sd). У 3 из 5 (60%) пациентов развивалась пневмония, а у 1 – сепсис. По шкале исходов Глазго (ШИГ) 4 балла было у 2 пациентов (наблюдение 4,11), 3 балла – у 2 пациентов (наблюдение 12,14), по ШИГ 1 балл – в 1 случае (наблюдение 2). Вероятно, исходы в III группы могли бы быть улучшены при своевременной реинтубации трахеи, что позволило бы избежать тяжелых инфекционно-воспалительных и септических осложнений. По данным литературы, нозокомиальная пневмония развивается вследствие аспирации при несвоевременной реинтубации трахеи у неуспешно эсктубированных пациентов [11,12,13,14,16,32].
Типичным пациентом этой группы является наблюдение 12.
Пациент Г, 31 год, поступил в Институт с диагнозом аневризма ПМА-ПСА справа, спонтанное субарахноидальное кровоизлияние с прорывом в желудочковую систему. При поступлении тяжесть состояния по шкале Хант-Хесс – III. Аневризма клипирована на 2 сутки после кровоизлияния. Послеоперационный период осложнился развитием ангиоспазма. В связи с этим проводилась пролонгированная седация и ИВЛ в течение 8 суток. Затем пациент экстубирован. По нашей шкале суммарная оценка составила 4 балла за счет снижения индекса рО2/FiО2 и умеренного беспокойства. Пациент был оставлен на самостоятельном дыхании. Постепенно нарастала тяжесть ДН, и через 3 часа пациент стал ажитированным, а индекс рО2/FiО2 снизился менее 200. Пациент был реинтубирован. Далее в течение последующих 6 суток проводилась ИВЛ через оротрахеальную трубку. Рентгенологически выявлялись прикорневые инфильтративные изменения, более выраженные справа. Пациент вновь был экстубирован на 7 сутки, суммарная оценка по шкале составила 5 баллов. Однако и в этот раз пациент был реинтубирован только через 1,5 часа, когда индекс рО2/FiО2 вновь снизился ниже 200 и появилась выраженная ажитация с агрессией (суммарная оценка – 7 баллов). ИВЛ через оротрахеальную трубку продолжалась еще 2 суток. Затем была выполнена трахеостомия. В дальнейшем у пациента развилась тяжелая ацинетобактерная пневмония и сепсис. В гемокультурах был также веделен ацинетобактер. На фоне проводимой интенсивной терапии удалось стабилизировать состояние. Пациент был переведен из отделения реанимации на 51 сутки, деканулирован на 53 сутки после трахеостомии, выписан из Института – на 65 сутки. По ШИГ – 3 балла.
Выводы:
- Созданная шкала, оценивающая: изменения сознания; нарушения глотания, кашля, свободной проходимости дыхательных путей; индекс рО2/FiО2 позволяет в оптимальные сроки произвести интубацию трахеи и возобновить ИВЛ.
- Суммарная оценка пациента в 4 и более баллов свидетельствует о ДН, требующей незамедлительного начала ИВЛ. При суммарном значении в 2 балла целесообразна оценка состояния пациента по шкале каждые 12 часов, а при 3 баллах – каждые 4-6 часов, или всякий раз при ухудшении состояния.
- Однократная оценка пациента позволяет установить непосредственную причину ДН, а динамическая оценка - определить последовательность изменения выраженности отдельных факторов, определяющих ДН.
- У пациентов с неуспешной экстубацией трахеи шкала позволит оптимизировать сроки реинтубации и, в результате, снизить частоту развития нозокомиальной и аспирационной пневмонии.
Список литературы.
- Горячев А.С., Савин И.А., Пуцилло М.В., Брагина Н.Н., Соколова Е.Ю., Щепетков А.Н., Фокин М.С., Кроптова М.В. Шкала оценки и терапевтическая стратегия при нарушении глотания у больных с повреждением ствола головного мозга. Вопросы нейрохирургии. 2006,4:24-28.
- Кассиль ВЛ, Выжигина МА, Лескин ГС Искусственная и вспомогательная вентиляция легких — М., 2004.
- Сатишур ОЕ Механическая вентиляция легких – М.,2006
- Afessa B, Gajic O, Keegan MT. Severity of illness and organ failure assessment in adult intensive care units. Crit Care Clin, 2007; 23(3): 639-658.
- Ambrosino N, Carpenè N, Gherardi M. Chronic respiratory care for neuromuscular diseases in adults. Eur Respir J. 2009; 34(2):444-451.
- Brain Trauma Foundation, Inc, American Association of Neurological Surgeons. Part 1: guidelines for the management of severe traumatic brain injury. New York (NY): Brain Trauma Foundation, Inc.; 2000. 165 p.
- Brain Trauma Foundation, American Association of Neurological Surgeons, Congress of Neurological Surgeons, Joint Section on Neurotrauma and Critical Care. Guidelines for the management of severe traumatic brain injury: cerebral perfusion pressure. New York (NY): Brain Trauma Foundation, Inc.; 2003 Mar 14. 14 p.
- Brain Trauma Foundation, American Association of Neurological Surgeons, Congress of Neurological Surgeons. Guidelines for the management of severe traumatic brain injury. Cerebral perfusion thresholds. J Neurotrauma 2007;24(Suppl 1):S59-S64.
- Brady SL, Pape TL, Darragh M, et al. Feasibility of instrumental swallowing assessments in patients with prolonged disordered consciousness while undergoing inpatient rehabilitation. J Head Trauma Rehabil. 2009, 24(5):384-91.
- Chang DW. Clinical application of mechanical ventilation. Thomson Delmar Learning, 2006, printed in Canada, third edition: p.216.
- Colonel P, Houzé MH, Vert H, et al. Swallowing Disorders as a Predictor of Unsuccessful Extubation: A Clinical Evaluation. American Journal of Critical Care. 2008;17(6):504-510.
- Coplin WM, Pierson DJ, Cooley KD, Newell DW, Rubenfeld GD. Implications of extubation delay in brain-injured patients meeting standard weaning criteria. Am J Respir Crit Care Med. 2000;161(5):1530-1536.
- Demling RH, Read T, Lind LJ, et al: Incidence and morbidity of extubation failure in surgical intensive care patients. Crit Care Med 1988; 16:573–577
- El Solh A, Okada M, Bhat A, Pietrantoni C. Swallowing disorders post orotracheal intubation in the elderly. Intensive Care Med. 2003;29(9):1451-1455.
- Ely EW, Truman B, Shintani A, et al. Monitoring sedation status over time in ICU patients: reliability and validity of the Richmond Agitation-Sedation Scale (RASS). JAMA. 2003, 11;289(22):2983-91.
- Epstein SK. Decision to extubate. Intensive Care Med. 2002; 28(5):535-546.
- Esteban A, Anzueto A, Frutos F, et al: Characteristics and outcomes in adult patients receiving mechanical ventilation: A 28-day international study. JAMA 2002; 287:345–355.
- Hamad GG, Peitzman AB. Morbid obesity and chronic intra-abdominal hypertension. From Abdominal compartment syndrome/edited by Ivatury RR, Cheatham ML, Malbrain, Sugrue M. Landes Bioscience, Texas, 2006:189-196.
- 2nd Edition New York: McGraw-Hill, 1996:120
- Lahrmann H, Wild M, Zdrahal F, Grisold W. Expiratory muscle weakness and assisted cough in ALS. Amyotroph Lateral Scler Other Motor Neuron Disord. 2003;4(1):49-51.
- Lazarus C, Logemann JA. Swallowing disorders in closed head trauma patients. Arch Phys Med Rehabil. 1987; 68(2):79-84.
- Leder SB, Espinosa JF. Aspiration risk after acute stroke: comparison of clinical examination and fiberoptic endoscopic evaluation of swallowing. Dysphagia. 2002;17(3):214-218.
- Logeman JA. Evaluation and Treatment of Swallowing Disorders. 2nd Edition, Texas, 1998.
- Lundy DS, Smith C, Colangelo L, et al. Aspiration: cause and implications. Otolaryngol Head Neck Surg. 1999;120(4): 474-478.
- Marshall JC, Cook DJ, Christou NV, et al. Multiple organ dysfunction score: a reliable description of a complex clinical outcome. Crit Care Med 1995;23(10):1638-1652.
- Martinez A, Seymour C, Nam M. Minute ventilation recovery time: A predictor of extubation outcome. Chest 2003;123:1214-1221.
- Navalesi P, Frigerio P, Moretti MP. Rate of reintubation in mechanically ventilated neurosurgical and neurologic patients: Evaluation of a systemic approach to weaning and extubation. Crit Care Med 2008, 36(11): 2986-2992.
- Pilbeam SP, Cairo JM. Mechanical Ventilation: Physiological and Clinical Applications 4th Edition, St Louis: Elsevier Mosby; 2006.
- Smina M, Salam A, Khamiees M, et al. Cough peak flows and extubation outcomes. Chest 2003;124:262-268
- Smith Hammond CA, Goldstein LB Cough and Aspiration of Food and Liquids Evidence-Based Clinical Practice Guidelines Due to Oral-Pharyngeal Dysphagia : ACCP Chest 2006;129;154S-168S
- Tobin MJ Principles and Practice of Mechanical Ventilation 2nd Edition. NewYork: McGraw Hill, 2006.
- Tolep K, Getch CL, Criner GJ. Swallowing dysfunction in patients receiving prolonged mechanical ventilation. Chest. 1996;109(1):167-172.
- Vallverdu I, Calaf N, Subirana M, et al: Clinical characteristics, respiratory functional parameters, and outcome of a two-hour Tpiece trial in patients weaning from mechanical ventilation. Am J Respir Crit Care Med 1998; 158:1855–1862
- Vincent JL, Moreno R, Takala J, et al. The SOFA (sepsis-related Organ Failure Assessment score to describe organ dysfunction/falure. On the behalf of the working group on sepsis-related promlems of the European society of intensive care medicine. Intensive Care Med 1999;22(7): 707-10.
- Zia WC. Coma and altered consciousness. From: Current clinical neurology: handbook of neurocritical care. Edited by Bhardwaj A, Mirski MA, Ulatowski JA. Humana Press Inc, Totowa, NJ, 2010.






