Введение
Гипернатриемия является частым вариантом электролитных нарушений в нейрохирургической практике [7]. У больных с аневризматическим субарахноидальным кровоизлиянием она развивается в 19 – 22%, у пострадавших с черепно-мозговой травмой – в 3 - 37%, а у пациентов после удаления опухолей хиазмально-селлярной области (ХСО) – более, чем в 60% [1;6;9;10;11]. Гипернатриемия, являясь прогностически неблагоприятным фактором, требует незамедлительной и адекватной коррекции [6;10]. Причинами гипернатриемии являются гиперкортицизм, гиперальдестеронизм, ограничение приема жидкости, дегидратация вседствие несахарного диабета, рвоты, диареи, гипергидроза [2]. Ятрогенная гипернатриемия описана при проведении осмотической терапии [7]. Методы коррекции гипернатриемии зависят прежде всего от причины ее развития, а инфузионная терапия является одним из основных компонентов проводимой интенсивной терапии вне зависимости от генеза гипернатриемии [3;5;8;9;13]. В нейрохирургической практике выбор базового инфузионного раствора является принципиальным. Известно, что растворы глюкозы противопоказаны в остром периоде [3;7]. Наиболее часто используемым кристаллоидным раствором на сегодня остается физиологический раствор. Однако его использование, особенно длительное и в большом объеме, сопряжено с развитием ряда побочных явлений [14]. В настоящее время доступны сбалансированные кристаллоидные растворы Стерофундин и Нормофундин. Применению этих растворов посвящена выполненная работа. Исследование проведено у больных после удаления опухолей ХСО, поскольку у них гипернатриемия развивается наиболее часто.
Материалы и методы
В исследование вошел 21 пациент с опухолями ХСО, у которых в раннем послеоперационном периоде развилась гипернатриемя.Пациенты были разделены на 3 группы. В первой группе (n=7) использовался физиологический раствор с добавлением в него 4% раствора хлорида калия (50 – 70 мл на 400 мл физ. раствора) и 25% раствора сульфата магния (10 – 15 мл на 400 мл физ. раствора). Во второй группе (n=7) использовали Нормофундин. В теретьей (n=7) – Стерофундин. Группы не отличались по возрасту и полу. В исследование вошли больные с аденомами гипофиза и краниофарингиомами. Пациентов с другими гистологическими вариантами в исследовании не было. Во всех наблюдениях выявлялся супраселлярный рост опухоли. Опухоли были или среднего размера, или гигантские. Не было выявлено отличий между группами в особенностях хирургических вмешательств и клинического состояния больных после операции. Не было различий в группах по выраженности гормональной недостаточности и по дозам использованных гормональных препаратов (ГДК + тиреоидные гормоны).Объем вводимой жидкости соответствовал сумме объемов базовых потребностей и объемов потерь жидкости. Для расчета суточной потребности пациента в жидкости было использовано следующее правило: масса тела условно была поделена на 1-10 кг, 11-20 кг и выше 20 кг: 1 - 10 кг (100 мл/кг) + 11 - 20 кг (50 мл/кг), + на каждый следующий кг (10 мл/кг). Все пациенты получали энтеральное питание сбалансированными смесями. Суточный объем питания вместе с водой сотавлял 2000 – 2500 мл. Раствор альбумина применялся для коррекции гипоальбуминемии. Гемотрансфузия проводилась при анемии (Hb<8 г/дл). Синтетические коллоидные препараты не использовались.Причиной гипернатриемии у исследуемой группы больных является несахарный диабет. Патогенетической терапией несахарного диабета является использования синтетических аналогов антидиуретического гормона – десмопрессина ацетата (Минирин). Дозу минирина подбирали по клиническому эффекту – до прекращения полиурии. В подавляющем большинстве наблюдений доза 0,2 мг минирина оказывалась эффективной. В 2 наблюдениях перавой группы и одном наблюдении второй группы требовались большие однократные дозы минирина – 0,4 мг. В течение исследования планово минирин не назначался. При натрии выше 155 ммоль/л гипотиазид. Остальной объем необходимой жидкости составили кристаллоидные растворы.
Физиологический раствор имеет осмолярность 308 ммосм/л. Однако содержание натрия и хлорида в нем превышает их нормальный уровень в плазме (154 ммоль/л). Кроме того, для восполнения часто встречающегося у реанимационных пациентов дефицита электролитов его приходится комбинировать с растворами KCl, MgSO4. Стерофундин сбалансирован по электролитному составу и изотоничен по отношению к плазме электролитным раствором. Входящие в его состав электролиты имеют концентрации, аналогичные таковым в плазме крови, за исключением хлорида (127 ммоль/л). Источником буферного бикарбоната (HCO3-) в Стерофундине является комбинация ацетата и малата, которые более предпочтительны в качестве носителей резервной щелочности, чем лактат. Кроме этого, обладая нулевым избытком оснований (BEpot), Стерофундин не изменяет кислотно-основной баланс пациента после введения. Нормофундин в сравнении с предыдущими растворами содержит принципиально меньшее количество натрия (100 ммоль/л) и хлорида (90 ммоль/л). Он содержит глюкозу (55 г/л), гипертоничен (530 мосм/л), имеет высокое содержания калия и магния (18 и 3 ммоль/л, соответственно). Буферным источником в Нормофундине является комбинация ацетата и производных хлористоводородной кислоты.При проведении инфузионной терапии в группах анализировались следующие параметры: Na в плазме, K в плазме, Cl, глюкоза, мочевина, рН, HCO3, ВЕ, осмолярность плазмы, Hb, Ht, протромбиновый индекс (ПТИ), активированное частично тромбопластиновое время (АЧТВ), количество тромбоцитов, Na в моче, K в моче, общий объем жидкости, объем кристаллоидного раствора, диурез, суточная доза минирина, суточная доза гипотиазида, ЦВД. Все лабораторные параметры, кроме показателей гемостаза, и ЦВД измеряли каждые 6 часов, остальные параметры, включая показатели гемостаза, – каждые 24 часа. Для статистического анализа использовали непараметрические методы (дисперсионный непараметрический анализ по Фридману, коэффициент конкордантности Кендалла, Хи-кв) [12]. Анализ полученных данных проводился по двум направлениям. Первое – это внутригрупповой анализ динамики каждого из параметров. Целью было выявление отклонений параметров от нормальных значений и определение статистически достоверных изменений в каждой группе. Для определения статистически достоверных изменений вычислялись р, коэффициент конкордантности и строился график динамики анализируемого параметра. Анализировались только те параметры, которые отличались от нормы или если изменения анализируемых параметров было достоверным (р<0.05, коэффициент конкордантности > 0.6, а графическое изображение динамики параметра не было синусоидным). Второе направление – это межгрупповой анализ параметров. Целью чего было выявление статистически достоверных различий в анализируемых параметрах между группами в последних четырех точках наблюдения (последние сутки исследования). Значения анализируемых параметров в выбранных точках должны отражать влияние инфузионных растворов на динамику этих параметров в течение исследования. Статистически достоверными считалось отличие, если р<0.017 (считались отличия с учетом поправки на множественные сравнения - 1/3 от 0.05).
Результаты исследования и их обсуждение
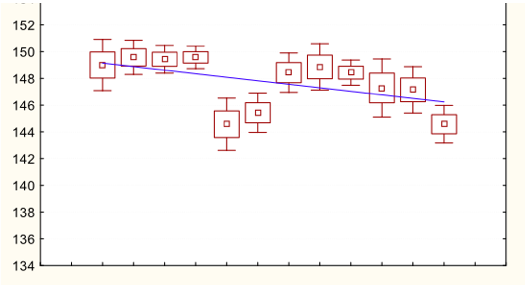
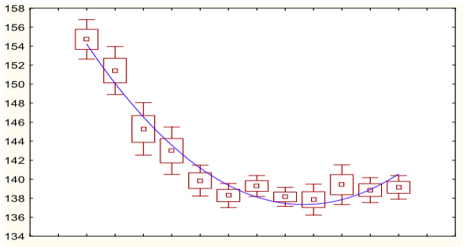
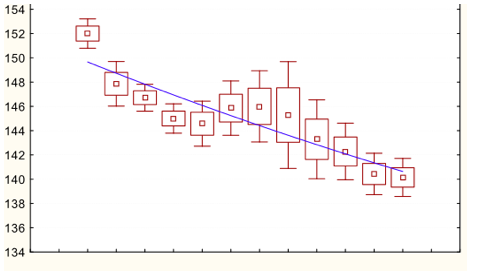
Уровень натрия плазмы снижался в динамике, достигая нормальных значений к временным срезам 4-5 (начало вторых суток), при использовании Нормофундина и Стерофундина. При использовании физиологического раствора сохранялась гипернатриемия фактически на протяжении всего периода исследования (Рисунки 1 – 3). Обращает на себя внимание, что при использовании Нормофундина уровень натрия ко вторым суткам снижался до нижней границе нормы, тогда как в группе со Стерофундином уровень натрия достигал верхней границы нормы.При анализе уровня натрия в последних четырех точках измерения было выявлено, что уровень натрия плазмы был ниже в группе с Нормофундином по сравнению с другими двумя группами во временном срезе 9 (начало третьих суток), а во временных срезах 10-12 концентрация натрия в плазме в группе с физиологическим раствором было выше, чем в двух других группах. Обращает на себя внимание гипернатриемия в группе с физиологическим раствором во временных срезах 10,11 (Рисунок 4).Таким образом, физиологический раствор был неэффективен для коррекции гипернатриемии. Стерофундин и Нормофундин были эффективно корригировали гипернатриемию, однако, безопасная коррекция была только в группе со Стерофундином. При использовании Нормофундина была отмечена быстрая и более выраженная коррекция уровня натрия плазмы, что повышает риск развития внутричерепной гипертензии при наличии отека мозга после операции [4].
Уровни калия и ВЕ в группах были в пределах нормы и фактически не изменялись в течение исследования.В группах с Нормофундином и физиологическим раствором была выявлена отчетливая тенденция к алкалозу. При анализе показателей рН в последних четырех точках исследования было выявлено, что рН был ниже в группе со Стерофундином по сравнению с другими двумя группами на временных срезах 9-12, а в t10 эта зависимость была статистически достоверна. Таким образом, только применение Стерофундина позволило корригировать алкалоз, характерный для раннего послеоперационного периода у больных с опухолями ХСО, и нормализовать рН к третьим суткам исследования. Причины сохраняющегося алкалоза в группе с физиологическим раствором, не смотря на гиперхлоремию, остаются непонятными.
В группе с Нормофундином и физиологическим раствором НСО3 был выше нормы фактически в течение всего периоде исследования в отличие от группы со Стерофундином. Однако статистически достоверных отличий в динамике НСО3 в группах не было.Гиперхлоремия в течение всего исследования была в группе с физиологическим раствором, что согласуется с данными других авторов [2;14]. В группе с Нормофундином уровень хлорида нормализовался к t5-6 (середина вторых суток), а в группе со Стерофундином – только к концу исследования. Таким образом, причиной алкалоза в группе с Нормофундином, было, во-первых, повышение концентрации бикарбоната в плазме вследствие специфического сочетания буферных соединений и их концентраций в Нормофундине и, во-вторых, низкое содержание хлора в этом растворе (90 ммоль/л). Причина алкалоза в группе с физиологическим раствором остается непонятной.Во всех группах была тенденция к гипергликемии без достоверных изменений в течение исследования. Концентрация мочевины увеличивалась при использовании Нормофундина. Причину этого феномена установить не удалось.Осмолярность плазмы достоверно снижалась при использовании Нормофундина, была тенденция к ее снижению при использовании Стерофундина, а в группе с физиологическим раствором не было выявлено статистически значимых изменений. Таким образом, использование Стерофундина в раннем послеоперационном периоде было наиболее безопасным, поскольку была получена тенденция к нормализации осмолярности, но отсутствовал риск нарастания послеоперационного отека, как это было в группе с Нормофундином. При использовании физиологического раствора осмолярность не изменялась в течение исследования.
Выводы
- Применение физиологического раствора не приводит к коррекции гипернатриемии. Применение Нормофундина сопряжено с риском быстрого и значимого снижения уровня натрия, вплоть до нижней границы нормы. При использовании Стерофундина возможно безопасная коррекция гипернатриемии.
- При использовании Стерофундина происходит коррекция алкалоза, характерного для пациентов с опухолями ХСО в раннем послеоперационном периоде. Нормофундин не способен корригировать алкалоз у этой группы больных, что определяется его составом. Применение физиологического раствора не приводило к нормализации кислотно-щелочного состояния.
- Уровень калия плазмы возможно поддерживать на нормальном уровне при использовании любого из растворов.
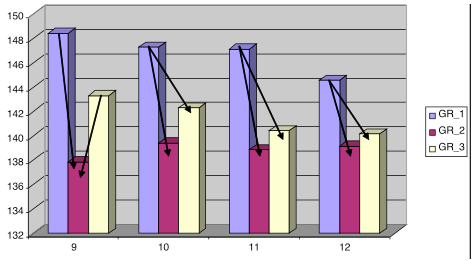
Примечание: GR1 – группа с физиологическим раствором, GR2 – группа с Нормофундином, GR3 – группа со Стерофундином.
Литература
- Аденомы гипофиза: клиника, диагностика, лечение. Под ред. Проф. Б.А.Кадашева. М.-Тверь: ООО «Издательство Триада», 2007: 368 стр.
- Морган Д.Э., Михаил М.С. Клиническая анестезиология. Москва, Санкт Петербург «Бином», «Невский диалект», 2000:365 стр.
- Томмасино К. Инфузионная терапия при пораженном мозге.// Российский журнал анестезиологии и интенсивной терапии. 1999; 2:68-70.
- Allan H. Ropper et al. Management of intracranial hypertension and mass effect, in Neurological and Neurosurgical Intensive Care. Lippincott Williams and Wilkins, 2004, 33-35.
- Cortbus F., Steudel W.I. Volume therapy in neurosurgery, in J.Treib (ed.): Volume Therapy. Berlin, Springer-Verlag, 2000, 60-68.
- Fisher LA, Ko N, Miss J, et al. Hypernatremia predicts adverse cardiovascular and neurological outcomes after SAH. Neurocrit. Care 2006;05:180-185.
- Greenberg M.S. “Handbook of neurosurgery”, Thieme, 2001, p.408, 419,136.
- Maroon J.C., Nelson P.B. Hypovolemia in patients with subarachnoid hemorrhage: Therapeutic implications. Neurosurgery. 1979; 4:223.
- Popugaev KA, Savin IA, Goriachev AS, Kadashev BA. Hypothalamic injury as a cause of refractory hypotension after sellar region tumor surgery. Neurocrit Care, 2008;8(3):366-73.
- Powner DJ, Boccalandro C, Alp MS, et al. Endocrine failure after traumatic brain injury in adults. Neurocrit. Care 2006;05:61-70.
- Qureshi AI, Suri MF, Sung CY, et al. Prognostic significance of hypernatremia and hyponatremia among patients with aneurysmal subarachnoid hemorrhage. Neurosurgery 2002;50:749-755; discusiion 755-756.
- Stanton A. Glantz. «Медико-математическая статистика». Перевод на русский язык, «Практика», 1998, v. 4.03.
- Solomon R.A., Post K.D., McMurtry J.G. Depression of circulating blood volume in patients after subarachnoid hemorrhage: Implications for the management of symptomatic vasospasm. Neurosurgery. 1984; 15:354-361.
- Zander R. Infusion fluids: why should they be balanced solution? EJHP Pract. 2006; 12:1-4.






