1.1 Самая простая классификация аппаратов ИВЛ (или о чём speech)
1.2 Респираторная механика – необходимый минимум
1.3 Повреждение легких при ИВЛ
2.1 Вступление ко второй части книги
2.3 Фазы дыхательного цикла и логика переключения аппарата ИВЛ
2.4 Что такое trigger (триггер), или как аппарат ИВЛ узнаёт, что пора начать вдох?
2.5 Предельные параметры вдоха (Limit variable)
2.8 Почувствуйте разницу (отличия программ работающих во время дыхательного цикла)
2.10 Паттерны ИВЛ Ventilatory Patterns
2.14 Использование принципа обратной связи в управлении аппаратом ИВЛ
2.15 Эволюция логических систем (принципов) управления аппаратом ИВЛ
2.16 Стратегия управления вдохом Control Strategy
3.2 Режимы вентиляции и терминологическая путаница
3.6 Pressure cycled ventilation
3.7 Pressure Support Ventilation
3.8 Intermittent Mandatory Ventilation + SIMV
3.9 Спонтанное дыхание на двух уровнях давления
3.10 Biphasic positive airway pressure
3.13 Mandatory minute ventilation
3.14 Dual Control Breath - введение
3.15 Dual control within a breath (VAPS и PLV)
Старики говорили нам: «Посадите пациента на ИВЛ, а потом не снимите». В чём-то они правы, - ИВЛ может повреждать легкие. В настоящее время проблеме VILI (ventilator induced lung injury) посвящено большое количество исследований. Наши земляки расшифровывают VILI как вентилятор индуцированное повреждение легких. Обсудим, какие варианты повреждения легких известны при ИВЛ.
Для того, чтобы предметно говорить об увлажнении, напомним определения физического понятия влажности. Абсолютная влажность (АВ) – это количество водяного пара, содержащегося в единице объёма газа (единица измерения – мг/л). Максимальная абсолютная влажность (МАВ) – это максимальное количество (мг/л) водяного пара для данной температуры газа или емкость газа для паров воды при данной температуре. Чем выше температура газа, тем больше максимальная абсолютная влажность. Насыщение газа водяным паром больше МАВ невозможно – происходит конденсация влаги в виде тумана и росы.
|
Соотношение максимальной абсолютной влажности и температуры воздуха
|
||||||||||
|
Температура С°
|
15
|
20
|
30
|
31
|
32
|
33
|
34
|
35
|
36
|
37
|
|
Макс. абсолютная
влажность мг/л
|
13
|
17
|
30
|
32
|
34
|
36
|
38
|
40
|
42
|
44
|
Относительная влажность (ОВ) – это отношение реальной абсолютной влажности газа к максимальной абсолютной влажности для данной температуры газа, выраженное в процентах (АВ/МАВ*100%)
|
Типичные значения температуры и влажности дыхательных газов
|
|||
|
|
Медицинские газы
(кислород)
|
Атмосферный
воздух
|
Воздух в легких
|
|
Температура С°
|
15
|
20
|
37
|
|
Относительная
влажность %
|
2
|
50
|
100
|
|
Абсолютная
влажность мг/л
|
0,5
|
12
|
44
|
У здорового человека при дыхании через нос происходит согревание воздуха до 37°С и увлажнение до 100% относительной влажности, что соответствует 44мг/л абсолютной влажности. Ежедневные потери здорового человека при самостоятельном дыхании через нос составляют приблизительно 250мл воды и 350ккал тепла в сутки. Важно отметить, что испарение происходит со слизистой оболочки носа и верхних дыхательных путей.
Мерцательный эпителий трахеи и бронхов представлен преимущественно цилиарными клетками (cilia – ресничка). Каждая такая клетка имеет 200-250 ресничек, которые колеблются с частотой 15/сек, непрерывно изгоняя бронхиальный секрет из дыхательных путей. Бронхиальный секрет продуцируют бокаловидные клетки эпителия и бронхиальные железы. Мерцательный эпителий трахеи и бронхов может эффективно работать только при нормальной вязкости бронхиального секрета.
В современных руководствах по ИВЛ [3, 4, 9, 10] вместо привычного термина увлажнение используется понятие «кондиционирование дыхательной смеси». Кондиционирование включает в себя очистку (фильтрацию), согревание и увлажнение дыхательной смеси.
Избыточное увлажнение приводит к конденсации влаги и разжижению секрета, - изгнание такого секрета требует большего количества движений ресничек.
Недостаток увлажнения дыхательной смеси приведёт повышению нагрузки на бронхиальные железы, избыточной потере воды - до 800мл и энергии - до 500ккал в сутки. При этом в отличие от нормальной физиологической ситуации, когда согревание и увлажнение вдыхаемого воздуха происходит в полости носа, - у интубированного или трахеостомированного пациента испарение происходит со слизистой оболочки трахеи и бронхов, что приводит к повышению вязкости бронхиального секрета. При достижении критического уровня вязкости цилиарные клетки оказываются не в состоянии удалять секрет из дыхательных путей. После этого цилиарные клетки утрачивают реснички. Очевидно, что нарушение эвакуации мокроты приводит к росту частоты воспалительных осложнений. Повреждение реснитчатого эпителия выявляются уже через 10 минут вентиляции сухим газом. Процесс восстановления ресничек длительный и энергозатратный. Длительность восстановления зависит от большого количества факторов и в каждом случае индивидуальна, но в среднем занимает 2-3 недели после восстановления влажности и нормальной температуры дыхательной смеси.
Важно отметить, что после того, как резервы увлажнения с поверхности трахеи и бронхов исчерпаны, и неувлажненный воздух достигает альвеол, начинается испарение с поверхности альвеол и происходит повреждение сурфактанта.
Вязкая мокрота налипает на стенки интубационной или трахеостомической трубки, сужая её просвет вплоть до полной обтурации. Таким образом, идеальное решение задачи кондиционирования дыхательной смеси выглядит так:
В ТРАХЕЮ ПАЦИЕНТА ДОЛЖНА ПОСТУПАТЬ ОЧИЩЕННАЯ ДЫХАТЕЛЬНАЯ СМЕСЬ 100% ВЛАЖНОСТИ НАГРЕТАЯ ДО 37°С.
Очевидно, холодные увлажнители барботажного и пульверизаторного типа не обеспечивают достаточного увлажнения и не согревают дыхательную смесь.
К сожалению, на основании собственного опыта и авторитетного мнения классиков [3, 4, 5, 7, 10] мы вынуждены отметить, что тепло-влагосберегающие фильтры для ИВЛ при великолепной фильтрации (в том числе антибактериальной) не обеспечивают необходимого увлажнения. Долгое время лучшими были нагревательные увлажнители типа «Benett» (аппараты ИВЛ Drager), где в закрытой емкости с большой поверхностью испарения автоматически поддерживается нужная температура воды. Недостатком этих увлажнителей является то, что при движении по шлангу дыхательного контура к пациенту дыхательная смесь несколько охлаждается, а влага конденсируется на стенках шлангов.
В настоящее время лучшими являются увлажнители – обогреватели, где в дополнение к емкости испарителя в шлангах проложен нагревающий провод. Благодаря системе автоматического поддержания температуры, получающей информацию из трех точек дыхательного контура, удаётся добиться оптимального увлажнения и согревания дыхательной смеси и избежать выпадения конденсата в дыхательном контуре (увлажнители Fisher&Pyker).
При спонтанном дыхании для уменьшения потерь тепла и влаги на трахеостомическую трубку необходимо надевать тепло-влагосберегающий фильтр («искусственный нос»), который достаточно эффективно кондиционирует дыхательную смесь, не ограничивая свободы пациента. Очень важно следить за проходимостью искусственного носа, который может забиваться слизью при кашле.
Приводим наиболее простую шкалу оценки вязкости бронхиального секрета
1. Жидкий – после аспирации мокроты санационный катетер чист.
2. Умеренно вязкий – после аспирации мокроты санационный катетер сразу очищается при промывании водой.
3. Вязкий – после аспирации мокроты санационный катетер трудно отмыть от мокроты.
Баротравма – это разрыв тканей легких или бронхов в ходе ИВЛ. Дословный перевод – повреждение давлением. Последствия разрыва → пневмоторакс или пневмомедиастенум → выключение части легких из газообмена и смещение средостения → гипоксия и нарушения гемодинамики → угроза жизни пациента.
Наиболее часто при ИВЛ баротравма происходит в зонах где альвеолы прилежат к бронхсосудистому ложу. Приведённая ниже иллюстрация взята из работы Maunder R J , Pierson D J, Hudson L D Subcutaneous and mediastinal emphysema: pathophisiology, diagnosis and managemtnt. Arch Intern Med 1984;144:1447-1453.
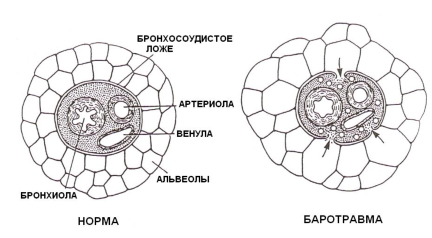
Какие силы могут разорвать лёгкие пациентa?
В разделе «Респираторная механика» мы предупреждали, что любое перемещение воздуха (ветер, ураган, вдох и выдох) возможно только за счет градиента давлений. Градиент давлений, критическое повышение которого может привести разрыву лёгких, называется – «Транспульмональный градиент давлений или Transpulmonary pressure gradient» Общепринятое сокращение – Pl. Транспульмональный градиент давлений составляет разность между альвеолярным и плевральным давлениями Pl = Palv – Ppl . Для краткости обычно используют термин «транспульмональное давление». (Если использована приставка «транс-» речь идёт о градиенте.)
Почему в барокамере, где создаётся давление в несколько атмосфер, не происходит разрыва легких?
Как ухитряется не погибнуть от пневмоторакса глубоководный водолаз? (Страшно сказать под каким давлением происходит вдох на глубине 10 метров, - на 1000смH2O выше атмосферного давления!)
Когда трубач дудит в свою трубу давление в дыхательных путях достигает 150 мбар много раз за концерт, а лёгкие не рвутся. Почему? На все эти вопросы ответ один: «Величина транспульмонального градиента давлений мала». В примерах с барокамерой и водолазом внешнее давление на грудную стенку и переднюю брюшную стенку уравновешивает давление в дыхательных путях и опасный градиент не возникает. Трубач сам создаёт давление за счёт усилия брюшного пресса и дыхательной мускулатуры и в тот момент, когда он дудит, лёгкие испытывают нагрузку на сжатие, а не на разрыв. Величина транспульмонального градиента давлений у трубача тоже мала и не опасна.
Практический вывод: Мы обязаны учитывать комплайнс (податливость) и/или ригидность (жесткость) грудной клетки и всей дыхательной системы, чтобы адекватно проводить ИВЛ и не ранить пациента. В ряде клинических ситуаций, у пациента с массивной, ригидной грудной клеткой только ИВЛ с высоким давлением позволит добиться адекватной вентиляции. В том случае, если податливость грудной клетки высокая, то при настройке режима ИВЛ следует защитить пациента от баротравмы, установив безопасный предел давления.
Дословный перевод – повреждение объёмом. Не порвали, а растянули. Как это получилось? Не было критического подъёма давления, однако потихонечку, аккуратненько в легкие было введено избыточное количество воздуха. Количество большее, чем лёгкие могут принять без повреждения. Альвеолы растянуты (перевод слова stretch), то есть повреждено большое количество альвеолярных мембран. Повреждение альвеолярных мембран приводит к повышению их проницаемости, накоплению внесосудистой воды в легких и выделению факторов системной воспалительной реакции (System inflammatory response syndrome SIRS). В 1988 году Дрейфус [Dreyfuss et all Am Rev Respir Dis 1988; 137:1159-1164] опубликовал результаты экспериментальной работы, выполненной на крысах. ИВЛ проводилась с высоким давлением. В контрольной группе выполнялось тугое бинтование грудной клетки. В экспериментальной группе не выполнялось. При ИВЛ с одинаковым давлением в обеих группах у животных с забинтованной грудной клеткой дыхательный объём не превышал физиологическую норму. В результате, в экспериментальной группе содержание внесосудистой воды в легких было в 3,5 раза больше, чем в контрольной. Основной вывод этой работы гласил: «При ИВЛ растяжение лёгких является критическим повреждающим фактором». «Lung stretch is the critical variable.»
Впервые описана в экспериментальной работе в 1974 году [Webb H H, Tierney D Experimental pulmonary edema due to positive pressure ventilation with high inflation pressures, protection by positive end-expiratory pressure. - Am Rev Respir Dis 1974;110:556-565] На фоне недостаточного или избыточного увлажнения, нарушенной эвакуации бронхиального секрета, воспалительных изменений меняется качество сурфактанта и эластические свойства легких. В результате, при полном выдохе часть альвеол слипается, то есть возникают ателектазы. При вдохе альвеолы вновь разлепляются. Этот феномен соответствует крепитации, выявляемой в экссудативные фазы острой пневмонии. В том случае, если в ходе ИВЛ в течение каждого дыхательного цикла происходит слипание и разлипание альвеол, возникает тяжелое повреждение легких. При слипании пневмоцитов, находящихся на противоположных стенках альвеолы, между оболочками этих клеток оказывается тонкий слой жидкости. При разлипании и раскрытии альвеолы между оболочками клеток возникает «мостик» из альвеолярного секрета. В тот момент, когда «мостик» рвётся высвобождается энергия и происходит разрыв клеточной стенки. Если за две минуты пневмоцит не успевает восстановить оболочку, он погибает. Обнажается альвеолярная мембрана. Повышается проницаемость альвеолярно-капиллярной стенки, и запускается механизм ответа на повреждение. То есть, привлечение макрофагов и выделение медиаторов воспаления. Одним словом – SIRS. Основной способ профилактики ателектотравмы - ИВЛ с использованием РЕЕР.
Биотравма – это повреждение легких факторами, вырабатываемыми собственным организмом. Биотравма легких наблюдается при сепсисе, шоке любой этиологии, тяжёлой травме и синдроме длительного сдавления (crash-syndrome), синдроме ДВС и иных состояниях, когда в венозном русле высока концентрация микроагрегатов, факторов системной воспалительной реакции и/или бактериальных токсинов. В этих ситуациях легкие выступают в роли фильтра, органа выделения и утилизации токсических продуктов. В настоящее время термину «шоковое легкое» соответствуют термины «ОПЛ острое повреждение легких» (ALI acute lung injury) и «ОРДС острый респираторный дистресс синдром» (ARDS acute respiratory distress syndrome).
Биотравма в контексте вентилятор индуцированного повреждения легких (VILI) –это выделение факторов системной воспалительной реакции в кровь и альвеолы на фоне агрессивной ИВЛ. Таким образом, агрессивная ИВЛ повреждает легкие не только за счет механического воздействия, но и как фактор провоцирующий выброс биологически активных веществ. Замыкается порочный круг. Формируется полиорганная недостаточность, усугубляются метаболические нарушения.
Токсичность кислорода была доказана в эксперименте на животных. При дыхании чистым кислородом смерть лабораторных животных наступала в сроки от 48 до 72 часов. Считается, что дыхание кислородом в высоких концентрациях приводит к формированию свободных радикалов. Эти свободные радикалы являются главным повреждающим фактором. У лабораторных животных, погибших при дыхании чистым кислородом, выявлялись повреждения легких идентичные ОПЛ. Здоровые добровольцы в эксперименте дышали чистым кислородом 24 часа. В результате, выявлены явления бронхита и воспалительные изменения в легких. Очевидно, что устойчивость человека к токсическому и повреждающему действию кислорода выше, чем у лабораторных животных. Есть лабораторные данные о том, что введение бактериального эндотоксина, воспалительных медиаторов и применение сублетальных концентраций кислорода (<85%) защищает легкие от дальнейшего повреждения при ингаляции кислорода. Таким образом многое еще не ясно. Общие рекомендации сводятся к следующему:
• Во всех ситуациях, когда завершена необходимая ИВЛ 100% кислородом (транспортировка, санация, периоды нестабильного состояния и т. д.), следует стремиться снижать концентрацию кислорода в дыхательной смеси.
• Относительно безопасной считается концентрация кислорода в дыхательной смеси <60%.
• Для большинства клинических ситуаций достижение РаО2 от 60 до 80mmHg является достаточным уровнем.
• Большинство клиницистов в ситуации выбора между гипоксемией или FIO2 >60% повышают концентрацию кислорода в дыхательной смеси.